Μιτοχονδριακό DNA
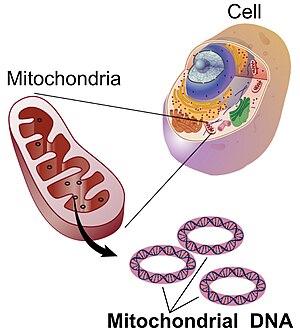
Το μιτοχονδριακό DNA (mitochondrial DNA ή mtDNA ή mDNA)[3] είναι το DNA που βρίσκεται στα μιτοχόνδρια, τα κυτταρικά οργανίδια μέσα σε ευκαρυωτικά κύτταρα που μετατρέπουν τη χημική ενέργεια από τα τρόφιμα σε μια μορφή που μπορούν να χρησιμοποιήσουν τα κύτταρα, την τριφωσφορική αδενοσίνη (ATP). Το μιτοχονδριακό DNA είναι μόνο ένα μικρό μέρος του DNA σε ένα ευκαρυωτικό κύτταρο. Το μεγαλύτερο μέρος του DNA μπορεί να βρεθεί στον κυτταρικό πυρήνα και σε φυτά και φύκια, επίσης σε πλαστίδια όπως χλωροπλάστες. Το ανθρώπινο μιτοχονδριακό DNA ήταν το πρώτο σημαντικό μέρος του ανθρώπινου γονιδιώματος που αλληλουχήθηκε.[4] Αυτή η αλληλούχιση αποκάλυψε ότι το ανθρώπινο mtDNA περιλαμβάνει 16.569 ζεύγη βάσεων και κωδικοποιεί 13 πρωτεΐνες.
Δεδομένου ότι το mtDNA των ζώων εξελίσσεται ταχύτερα από τους πυρηνικούς γενετικούς δείκτες,[5][6][7] αντιπροσωπεύει έναν στυλοβάτη της φυλογένεσης και της εξελικτικής βιολογίας. Επιτρέπει επίσης την εξέταση της συγγένειας των πληθυσμών, και έτσι έχει γίνει σημαντική στην ανθρωπολογία και την βιογεωγραφία.
Προέλευση Επεξεργασία
Το πυρηνικό και το μιτοχονδριακό DNA θεωρείται ότι έχουν ξεχωριστή εξελικτική προέλευση, με το mtDNA να προέρχεται από τα κυκλικά γονιδιώματα βακτηρίων που περιβλήθηκαν από τους πρώτους προγόνους των σημερινών ευκαρυωτικών κυττάρων. Αυτή η θεωρία ονομάζεται ενδοσυμβιωτική θεωρία. Στα κύτταρα των υφιστάμενων οργανισμών, η συντριπτική πλειοψηφία των πρωτεϊνών που υπάρχουν στα μιτοχόνδρια (αριθμούν περίπου 1500 διαφορετικούς τύπους στα θηλαστικά) κωδικοποιούνται από το πυρηνικό DNA, αλλά τα γονίδια για ορισμένες, αν όχι τις περισσότερες, πιστεύεται ότι είχαν αρχικά βακτηριακή προέλευση, αφού από τότε μεταφέρθηκαν στον πυρήνα ευκαρυωτικών κυττάρων κατά τη διάρκεια της εξέλιξης.[8]
Οι λόγοι για τους οποίους τα μιτοχόνδρια έχουν διατηρήσει ορισμένα γονίδια αμφισβητούνται. Η ύπαρξη σε ορισμένα είδη οργανιδίων που παράγονται από μιτοχόνδρια που τους λείπει το γονιδίωμα[9] προτείνει ότι είναι δυνατή η πλήρης απώλεια γονιδίων και η μεταφορά μιτοχονδριακών γονιδίων στον πυρήνα και έχει αρκετά πλεονεκτήματα.[10] Η δυσκολία στόχευσης προϊόντων υδρόφοβων πρωτεϊνών που παράγονται εξ αποστάσεως στο μιτοχόνδριο είναι μια υπόθεση για το γιατί ορισμένα γονίδια διατηρούνται στο mtDNA.[11] Η υπόθεση CoRR είναι μία άλλη, που αναφέρεται στην επιθυμία του εντοπισμένου ελέγχου επί των μιτοχονδριακών μηχανημάτων.[12] Πρόσφατη ανάλυση ευρέος φάσματος γονιδιωμάτων του mtDNA προτείνει ότι και τα δύο αυτά χαρακτηριστικά μπορεί να υπαγορεύουν τη διατήρηση μιτοχονδριακού γονιδίου.[8]
Δομή και ποικιλομορφία γονιδιώματος Επεξεργασία
Σε όλους τους οργανισμούς, υπάρχουν έξι κύριοι τύποι γονιδιώματος που βρίσκονται στα μιτοχονδριακά γονιδιώματα, ταξινομημένοι ανάλογα με τη δομή τους (δηλ. κυκλικοί έναντι γραμμικών), το μέγεθος, την παρουσία εσωνίων ή δομών τύπου πλασμιδίου και εάν το γενετικό υλικό είναι ένα μοναδικό μόριο ή συλλογή ομοιογενών ή ετερογενών μορίων.[13]
Σε πολλούς μονοκύτταρους οργανισμούς (π.χ. βλεφαριδοφόρο τετραϋμένα και πράσινο φύκι Χλαμυδομονάς του Ράινχαρτ) και σε σπάνιες περιπτώσεις επίσης σε πολυκύτταρους οργανισμούς (π.χ. σε ορισμένα είδη κνιδοζώων), το mtDNA βρίσκεται ως γραμμικά οργανωμένο DNA. Τα περισσότερα από αυτά τα γραμμικά mtDNA διαθέτουν -ανεξάρτητα τελομερή (δηλαδή, τα άκρα του γραμμικού DNA) με διαφορετικούς τρόπους αντιγραφής, που τους έχουν κάνει ενδιαφέροντα αντικείμενα έρευνας επειδή αυτοί οι μονοκύτταροι οργανισμοί με γραμμικό mtDNA είναι γνωστοί παθογόνοι παράγοντες. [14]
Ζώα Επεξεργασία
Τα περισσότερα ζώα, ειδικά τα διμερή ζώα, έχουν κυκλικό μιτοχονδριακό γονιδίωμα. Οι κλάδοι μεδουσόζωα (Medusozoa) και ασβεστόσπογγοι ωστόσο έχουν είδη με γραμμικά μιτοχονδριακά χρωμοσώματα.[15]
Όσον αφορά τα ζεύγη βάσεων, η ανεμώνη Isarachnanthus nocturnus έχει το μεγαλύτερο μιτοχονδριακό γονιδίωμα από οποιοδήποτε ζώο με 80.923 bp. [16]
Τον Φεβρουάριο του 2020, ανακαλύφθηκε ένα παράσιτο που σχετίζεται με τις μέδουσες- Henneguya salminicola - που στερούνται μιτοχονδριακού γονιδιώματος αλλά διατηρούν δομές που θεωρούνται οργανίδια που σχετίζονται με μιτοχόνδρια. Επιπλέον, τα γονίδια πυρηνικού DNA που εμπλέκονται στην αερόβια αναπνοή και στην αντιγραφή και μεταγραφή του μιτοχονδριακού DNA είτε απουσίαζαν είτε παρουσιάζονταν μόνο ως ψευδογονίδια. Αυτός είναι ο πρώτος πολυκυτταρικός οργανισμός που είναι γνωστό ότι έχει αυτήν την απουσία αερόβιας αναπνοής και ζει εντελώς απαλλαγμένος από εξάρτηση από οξυγόνο.[17][18]
Φυτά και μύκητες Επεξεργασία
Υπάρχουν τρεις διαφορετικοί τύποι μιτοχονδριακού γονιδιώματος που βρίσκονται σε φυτά και μύκητες. Ο πρώτος τύπος είναι ένα κυκλικό γονιδίωμα που έχει εσώνια (τύπου 2) και μπορεί να κυμαίνεται από 19 έως 1000 kbp σε μήκος. Ο δεύτερος τύπος γονιδιώματος είναι ένα κυκλικό γονιδίωμα (περίπου 20–1000 kbp) που έχει επίσης δομή που μοιάζει με πλασμίδιο (1 kb) (τύπος 3). Ο τελευταίος τύπος γονιδιώματος που μπορεί να βρεθεί σε φυτά και μύκητες είναι ένα γραμμικό γονιδίωμα που αποτελείται από ομοιογενή μόρια DNA (τύπος 5).
Υπάρχει μεγάλη ποικιλία στο περιεχόμενο και το μέγεθος του γονιδίου mtDNA μεταξύ των μυκήτων και των φυτών, αν και φαίνεται να υπάρχει ένα βασικό υποσύνολο γονιδίων που υπάρχουν σε όλα τα ευκαρυωτικά (εκτός από τα λίγα που δεν έχουν καθόλου μιτοχόνδρια).[8] Ορισμένα είδη φυτών έχουν τεράστια μιτοχονδριακά γονιδιώματα, με το mtDNA του Silene conica να περιέχει έως και 11.300.000 ζεύγη βάσεων.[19] Παραδόξως, ακόμη και αυτά τα τεράστια mtDNA περιέχουν τον ίδιο αριθμό και είδη γονιδίων με τα σχετικά φυτά με πολύ μικρότερα mtDNA.[20] Το γονιδίωμα του μιτοχονδρίου του αγγουριού (Cucumis sativus) αποτελείται από τρία κυκλικά χρωμοσώματα (μήκη 1556, 84 και 45 χιλιάδες βάσεων), τα οποία είναι πλήρως ή σε μεγάλο βαθμό αυτόνομα όσον αφορά την αναπαραγωγή.[21]
Πρώτιστα Επεξεργασία
Τα πρώτιστα περιέχουν τα πιο διαφορετικά μιτοχονδριακά γονιδιώματα, με πέντε διαφορετικούς τύπους σε αυτό το βασίλειο. Ο τύπος 2, ο τύπος 3 και ο τύπος 5 που αναφέρονται στα γονιδιώματα των φυτών και των μυκήτων υπάρχουν επίσης σε ορισμένα πρώτιστα, όπως και δύο μοναδικοί τύποι γονιδιώματος. Ένας από αυτούς τους μοναδικούς τύπους είναι μια ετερογενής συλλογή μορίων κυκλικού DNA (τύπος 4), ενώ ο άλλος είναι μια ετερογενής συλλογή γραμμικών μορίων (τύπος 6). Οι τύποι γονιδιώματος 4 και 6 ο καθένας κυμαίνονται από 1–200 kbp σε μέγεθος.
Το μικρότερο μιτοχονδριακό γονιδίωμα που έχει αλληλουχηθεί μέχρι σήμερα είναι 5.967 bp mtDNA του παρασίτου Plasmodium falciparum.[22][23]
Η ενδοσυμβιωτική γονιδιακή μεταφορά, η διαδικασία με την οποία τα γονίδια που κωδικοποιήθηκαν στο μιτοχονδριακό γονιδίωμα μεταφέρονται στο κύριο γονιδίωμα του κυττάρου, πιθανότατα εξηγεί γιατί πιο σύνθετοι οργανισμοί όπως ο άνθρωπος έχουν μικρότερα μιτοχονδριακά γονιδιώματα από τους απλούστερους οργανισμούς όπως τα πρώτιστα.
| Τύπος γονιδιώματος[13] | Βασίλειο | Εσώνια | Μέγεθος | Σχήμα | Περιγραφή |
|---|---|---|---|---|---|
| 1 | Ζώα | Όχι | 11–28 kbp | Κυκλικά | Μονομοριακά |
| 2 | Μύκητες, φυτά, πρώτιστα | Ναι | 19–1000 kbp | Κυκλικά | Μονομοριακά |
| 3 | Μύκητες, φυτά, πρώτιστα | Όχι | 20–1000 kbp | Κυκλικά | Μεγάλα μόρια και μικρά πλασμίδια όπως δομές |
| 4 | Πρώτιστα | Όχι | 1–200 kbp | Κυκλικά | Ετερογενής ομάδα μορίων |
| 5 | Μύκητες, φυτά, πρώτιστα | Όχι | 1–200 kbp | Γραμμικά | Ομοιογενής ομάδα μορίων |
| 6 | Πρώτιστα | Όχι | 1–200 kbp | Γραμμικά | Ετερογενής ομάδα μορίων |
Αναπαραγωγή Επεξεργασία
Το μιτοχονδριακό DNA αντιγράφεται από το σύμπλεγμα γάμμα της πολυμεράσης DNA το οποίο αποτελείται από καταλυτική πολυμεράση DNA 140 kDa κωδικοποιημένη από το γονίδιο POLG και δύο βοηθητικές υπομονάδες 55 kDa που κωδικοποιούνται από το γονίδιο POLG2.[24] Ο μηχανισμός αντιγραφοσώματος σχηματίζεται από πολυμεράση DNA, TWINKLE και μιτοχονδριακές πρωτεΐνες SSB (που δεσμεύονται σε μονόκλωνο DNA). Το TWINKLE είναι μία ελικάση, που ξετυλίγει μικρές εκτάσεις dsDNA στην κατεύθυνση 5' προς 3'.[25] Όλα αυτά τα πολυπεπτίδια κωδικοποιούνται στο πυρηνικό γονιδίωμα.
Κατά τη διάρκεια της εμβρυογένεσης, η αντιγραφή του mtDNA υπορρυθμίζεται αυστηρά από το γονιμοποιημένο ωάριο μέσω του προεμφυτευτικού εμβρύου.[26] Η προκύπτουσα μείωση του αριθμού αντιγράφων ανά κύτταρο του mtDNA παίζει ρόλο στη στενωπό του μιτοχονδρίου, αξιοποιώντας μεταβλητότητα από κύτταρο σε κύτταρο για τη βελτίωση της κληρονομικότητας των επιβλαβών μεταλλάξεων.[27] Σύμφωνα με τον Justin St. John και τους συνεργάτες του, "Στο στάδιο βλαστοκύστης, η έναρξη της αντιγραφής του mtDNA είναι ειδική για τα κύτταρα του τροφοεκτοδέρματος.[26] Αντίθετα, τα κύτταρα της εσωτερικής κυτταρικής μάζας (inner cell mass) περιορίζουν την αντιγραφή του mtDNA μέχρι να λάβουν τα σήματα για να διαφοροποιηθούν σε συγκεκριμένους τύπους κυττάρων."[26]
Γονίδια στο ανθρώπινο mtDNA και η μεταγραφή τους Επεξεργασία
Οι δύο αλυσίδες του ανθρώπινου μιτοχονδριακού DNA διακρίνονται ως η βαριά και η ελαφριά αλυσίδα. Η βαριά αλυσίδα είναι πλούσια σε γουανίνη και κωδικοποιεί 12 υπομονάδες του συστήματος οξειδωτικής φωσφορυλίωσης, δύο ριβοσωμικά RNA (12S και 16S) και 14 tRNA. Η ελαφριά αλυσίδα κωδικοποιεί μία υπομονάδα και 8 tRNA. Έτσι, συνολικά το mtDNA κωδικοποιεί δύο rRNA, 22 tRNA και 13 υπομονάδες πρωτεϊνών, που όλες τους εμπλέκονται στη διαδικασία της οξειδωτικής φωσφορυλίωσης.[28][29]
| Γονίδιο | Τύπος | Προϊόν | Θέσεις στο μιτογονιδίωμα |
Κλώνος |
|---|---|---|---|---|
| MT-ATP8 | Κωδικοποίηση πρωτεΐνης | Συνθάση ATP, Fo υπομονάδα 8 (σύμπλοκο V) | 08,366–08,572 (επικάλυψη με MT-ATP6) | H |
| MT-ATP6 | Κωδικοποίηση πρωτεΐνης | Συνθάση ATP, Fo υπομονάδα 6 (σύμπλοκο V) | 08,527–09,207 (επικάλυψη με MT-ATP8) | H |
| MT-CO1 | Κωδικοποίηση πρωτεΐνης | Οξειδάση του κυτοχρώματος c, υπομονάδα 1 (σύμπλοκο IV) | 05,904–07,445 | H |
| MT-CO2 | Κωδικοποίηση πρωτεΐνης | Οξειδάση του κυτοχρώματος c, υπομονάδα 2 (σύμπλοκο IV) | 07,586–08,269 | H |
| MT-CO3 | Κωδικοποίηση πρωτεΐνης | Οξειδάση του κυτοχρώματος c, υπομονάδα 3 (σύμπλοκο IV) | 09,207–09,990 | H |
| MT-CYB | Κωδικοποίηση πρωτεΐνης | Κυτόχρωμα b (σύμπλοκο III) | 14,747–15,887 | H |
| MT-ND1 | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 1 (σύμπλοκο I) | 03,307–04,262 | H |
| MT-ND2 | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 2 (σύμπλοκο I) | 04,470–05,511 | H |
| MT-ND3 | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 3 (σύμπλοκο I) | 10,059–10,404 | H |
| MT-ND4L | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 4L (σύμπλοκο I) | 10,470–10,766 (overlap with MT-ND4) | H |
| MT-ND4 | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 4 (σύμπλοκο I) | 10,760–12,137 (overlap with MT-ND4L) | H |
| MT-ND5 | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 5 (σύμπλοκο I) | 12,337–14,148 | H |
| MT-ND6 | Κωδικοποίηση πρωτεΐνης | Αφυδρογονάση NADH, υπομονάδα 6 (σύμπλοκο I) | 14,149–14,673 | L |
| MT-RNR2 | Κωδικοποίηση πρωτεΐνης | Ουμανίνη | — | — |
| MT-TA | Μεταφορικό RNA | tRNA-Αλανίνης (Ala ή A) | 05,587–05,655 | L |
| MT-TR | Μεταφορικό RNA | tRNA-Αργινίνης (Arg ή R) | 10,405–10,469 | H |
| MT-TN | Μεταφορικό RNA | tRNA-Ασπαραγίνης (Asn ή N) | 05,657–05,729 | L |
| MT-TD | Μεταφορικό RNA | tRNA-ασπαραγινικού οξέος (Asp ή D) | 07,518–07,585 | H |
| MT-TC | Μεταφορικό RNA | tRNA-Κυστεΐνης (Cys ή C) | 05,761–05,826 | L |
| MT-TE | Μεταφορικό RNA | tRNA-Γλουταμινικού οξέος (Glu ή E) | 14,674–14,742 | L |
| MT-TQ | Μεταφορικό RNA | tRNA-Γλουταμίνης (Gln ή Q) | 04,329–04,400 | L |
| MT-TG | Μεταφορικό RNA | tRNA-Γλυκίνης (Gly ή G) | 09,991–10,058 | H |
| MT-TH | Μεταφορικό RNA | tRNA-Ιστιδίνης (His ή H) | 12,138–12,206 | H |
| MT-TI | Μεταφορικό RNA | tRNA-Ισολευκίνης (Ile ή I) | 04,263–04,331 | H |
| MT-TL1 | Μεταφορικό RNA | tRNA-Λευκίνης (Leu-UUR ή L) | 03,230–03,304 | H |
| MT-TL2 | Μεταφορικό RNA | tRNA-Λευκίνης (Leu-CUN ή L) | 12,266–12,336 | H |
| MT-TK | Μεταφορικό RNA | tRNA-Λυσίνης (Lys ή K) | 08,295–08,364 | H |
| MT-TM | Μεταφορικό RNA | tRNA-Μεθειονίνης (Met ή M) | 04,402–04,469 | H |
| MT-TF | Μεταφορικό RNA | tRNA-Φαινυλαλανίνης (Phe ή F) | 00,577–00,647 | H |
| MT-TP | Μεταφορικό RNA | tRNA-Προλίνης (Pro ή P) | 15,956–16,023 | L |
| MT-TS1 | μεταφορικό RNA | tRNA-Σερίνης (Ser-UCN ή S) | 07,446–07,514 | L |
| MT-TS2 | Μεταφορικό RNA | tRNA-Σερίνης (Ser-AGY ή S) | 12,207–12,265 | H |
| MT-TT | Μεταφορικό RNA | tRNA-Θρεονίνης (Thr ή T) | 15,888–15,953 | H |
| MT-TW | Μεταφορικό RNA | tRNA-Τρυπτοφάνης (Trp ή W) | 05,512–05,579 | H |
| MT-TY | Μεταφορικό RNA | tRNA-Τυροσίνης (Tyr ή Y) | 05,826–05,891 | L |
| MT-TV | Μεταφορικό RNA | tRNA-Βαλίνης (Val ή V) | 01,602–01,670 | H |
| MT-RNR1 | Ριβοσωμικό RNA | Μικρή υπομονάδα : SSU (12S) | 00,648–01,601 | H |
| MT-RNR2 | Ριβοσωμικό RNA | Μεγάλη υπομονάδα : LSU (16S) | 01,671–03,229 | H |
Μεταξύ των περισσοτέρων (αλλά όχι όλων) των περιοχών που κωδικοποιούν πρωτεΐνες, υπάρχουν tRNA (δείτε τον χάρτη του ανθρώπινου μιτοχονδριακού γονιδιώματος). Κατά τη μεταγραφή, τα tRNA αποκτούν το χαρακτηριστικό τους σχήμα L που αναγνωρίζεται και διασπάται από συγκεκριμένα ένζυμα. Με την επεξεργασία του μιτοχονδριακού RNA, μεμονωμένες αλληλουχίες mRNA, rRNA και tRNA απελευθερώνονται από την κύρια μεταγραφή.[31] [32] Τα αναδιπλωμένα tRNA συνεπώς, λειτουργούν ως σημεία δευτεροταγούς δομής.[33]
Ρύθμιση της μεταγραφής Επεξεργασία
Οι υποκινητές για την έναρξη της μεταγραφής των βαριών και ελαφριών αλυσίδων βρίσκονται στην κύρια μη κωδικοποιητική περιοχή του mtDNA που ονομάζεται βρόχος μετατόπισης, ο βρόχος D.[28] Υπάρχουν ενδείξεις ότι η μεταγραφή των μιτοχονδριακών rRNA ρυθμίζεται από τον προαγωγό βαρέων αλυσίδων 1 (HSP1) και η μεταγραφή των πολυσιστρονικών μεταγραφών που κωδικοποιούν τις πρωτεϊνικές υπομονάδες ρυθμίζεται από το HSP2.[28]
Η μέτρηση των επιπέδων των κωδικοποιημένων με mtDNA RNA σε ιστούς βοοειδών έδειξε ότι υπάρχουν σημαντικές διαφορές στην έκφραση των μιτοχονδριακών RNA σε σχέση με το ολικό RNA ιστού.[34] Μεταξύ των 12 ιστών που εξετάστηκαν το υψηλότερο επίπεδο έκφρασης παρατηρήθηκε στην καρδιά, ακολουθούμενο από δείγματα εγκεφαλικού και στεροειδογενετικού ιστού. [34]
Όπως αποδεικνύεται από την επίδραση της τροφικής ορμόνης ACTH στα κύτταρα του φλοιού των επινεφριδίων, η έκφραση των μιτοχονδριακών γονιδίων μπορεί να ρυθμίζεται έντονα από εξωτερικούς παράγοντες, προφανώς για να ενισχύσει τη σύνθεση των μιτοχονδριακών πρωτεϊνών που είναι απαραίτητες για την παραγωγή ενέργειας. [34] Είναι ενδιαφέρον, ότι ενώ η έκφραση των γονιδίων που κωδικοποιούν πρωτεΐνες διεγέρθηκε από ACTH, τα επίπεδα του μιτοχονδριακού 16S rRNA δεν έδειξαν σημαντική αλλαγή.[34]
Μιτοχονδριακή κληρονομικότητα Επεξεργασία
Στους περισσότερους πολυκύτταρους οργανισμούς, το mtDNA κληρονομείται από τη μητέρα (μητρική κληρονομικότητα). Οι μηχανισμοί για αυτό περιλαμβάνουν απλή αραίωση (ένα ωάριο περιέχει κατά μέσο όρο 200.000 μόρια mtDNA, ενώ το σπέρμα ενός υγιούς ανθρώπου έχει αναφερθεί ότι περιέχει κατά μέσο όρο 5 μόρια), [35][36] αποικοδόμηση του mtDNA του σπέρματος στην ανδρική γεννητική οδό και στο γονιμοποιημένο ωάριο, και τουλάχιστον σε μερικούς οργανισμούς, αποτυχία του mtDNA του σπέρματος να εισέλθει στο ωάριο. Όποιος κι αν είναι ο μηχανισμός, αυτό το μοτίβο γονέα (μονογονική κληρονομιά) όσον αφορά την κληρονομικότητα του mtDNA βρίσκεται στα περισσότερα ζώα, στα περισσότερα φυτά και επίσης στους μύκητες.
Σε εξαιρετικές περιπτώσεις, τα ανθρώπινα μωρά κληρονομούν μερικές φορές mtDNA τόσο από τους πατέρες όσο και από τις μητέρες τους με αποτέλεσμα την ετεροπλασμία του mtDNA.[37]
Θηλυκή κληρονομικότητα Επεξεργασία
Στη φυλετική αναπαραγωγή, τα μιτοχόνδρια κληρονομούνται κανονικά αποκλειστικά από τη μητέρα. Τα μιτοχόνδρια στο σπέρμα των θηλαστικών συνήθως καταστρέφονται από το ωάριο μετά τη γονιμοποίηση. Επίσης, τα μιτοχόνδρια βρίσκονται μόνο στην ουρά του σπέρματος, η οποία χρησιμοποιείται για την προώθηση των σπερματοζωαρίων και μερικές φορές η ουρά χάνεται κατά τη γονιμοποίηση. Το 1999 αναφέρθηκε ότι τα μιτοχόνδρια του πατρικού σπέρματος (που περιέχουν mtDNA) φέρουν σήμανση με ουμπικουιτίνη για να τα επιλέξουν για μελλοντική καταστροφή μέσα στο έμβρυο.[38] Ορισμένες τεχνικές γονιμοποίησης στο εργαστήριο, ιδιαίτερα η έγχυση σπέρματος σε ωάριο, μπορεί να επέμβη σε αυτό.
Το γεγονός ότι το μιτοχονδριακό DNA κληρονομείται κυρίως από τη μητέρα επιτρέπει στους γενεαλογικούς ερευνητές να εντοπίσουν τη μητρική καταγωγή πολύ πίσω στον χρόνο. Το (Υ-χρωμοσωμικό DΝΑ, που κληρονομείται από τον πατέρα, χρησιμοποιείται με ανάλογο τρόπο για τον προσδιορισμό της πατρογονικής ιστορίας. Αυτό συνήθως επιτυγχάνεται στο ανθρώπινο μιτοχονδριακό DNA με αλληλούχιση των υπερμεταβλητών περιοχών ελέγχου (HVR1 ή HVR2), και μερικές φορές το πλήρες μόριο του μιτοχονδριακού DNA, ως γενεαλογικό τεστ DNA.[39] Το HVR1, για παράδειγμα, αποτελείται από περίπου 440 ζεύγη βάσεων. Αυτά τα 440 ζεύγη βάσεων συγκρίνονται με τις ίδιες περιοχές άλλων ατόμων (είτε συγκεκριμένων ατόμων, είτε υποκειμένων σε μια βάση δεδομένων) για τον προσδιορισμό της μητρικής καταγωγής. Τις περισσότερες φορές, η σύγκριση γίνεται με την αναθεωρημένη Ακολουθία Αναφοράς Cambridge. Ο Vilà κ.α. έχουν δημοσιεύσει μελέτες εντοπισμού της μητρικής καταγωγής κατοικίδιων σκύλων από λύκους.[40] Η ιδέα της μιτοχονδριακής Εύας βασίζεται στον ίδιο τύπο ανάλυσης, προσπαθώντας να ανακαλύψει την προέλευση της ανθρωπότητας παρακολουθώντας την καταγωγή πίσω στο παρελθόν.
Η μιτοχονδριακή στενωπός Επεξεργασία
Οι οντότητες που υπόκεινται σε μονογονική κληρονομικότητα και με ελάχιστο ή καθόλου ανασυνδυασμό μπορεί να αναμένεται ότι υπόκεινται στην καστάνια του Μίλερ, τη συσσώρευση επιβλαβών μεταλλάξεων έως ότου χαθεί η λειτουργικότητα. Οι ζωικοί πληθυσμοί των μιτοχονδρίων το αποφεύγουν μέσω μιας αναπτυξιακής διαδικασίας γνωστής ως στενωπός του mtDNA. Η στενωπός εκμεταλλεύεται τις τυχαίες διεργασίες στο κύτταρο για να αυξήσει τη μεταβλητότητα κυττάρων σε κύτταρα στο μεταλλαγμένο φορτίο καθώς αναπτύσσεται ένας οργανισμός: ένα μόνο ωάριο με κάποια αναλογία μεταλλαγμένου mtDNA παράγει έτσι ένα έμβρυο στο οποίο διαφορετικά κύτταρα έχουν διαφορετικά μεταλλαγμένα φορτία. Η επιλογή επιπέδου κυττάρου μπορεί στη συνέχεια να δράσει για την αφαίρεση αυτών των κυττάρων με περισσότερο μεταλλαγμένο mtDNA, οδηγώντας σε σταθεροποίηση ή μείωση του μεταλλαγμένου φορτίου μεταξύ γενεών. Ο μηχανισμός που διέπει τη στενωπό αμφισβητείται, [41][42][43][44] με μια πρόσφατη μαθηματική και πειραματική μεταμελέτη που παρέχει στοιχεία για συνδυασμό τυχαίας κατάτμησης των mtDNAs σε κυτταρικές διαιρέσεις και τυχαίο κύκλο μορίων mtDNA εντός του κυττάρου.[27]
Αρσενική κληρονομικότητα Επεξεργασία
Η αρσενική κληρονομικότητα μιτοχονδριακού DNA έχει ανακαλυφθεί στα κοτόπουλα Plymouth Rock.[45] Τα στοιχεία υποστηρίζουν σπάνιες περιπτώσεις αρσενικής μιτοχονδριακής κληρονομικότητας σε ορισμένα θηλαστικά επίσης. Συγκεκριμένα, υπάρχουν τεκμηριωμένα περιστατικά για ποντίκια,[46][47] όπου τα αρσενικά κληρονομικά μιτοχόνδρια απορρίφθηκαν στη συνέχεια. Έχει επίσης βρεθεί σε πρόβατα,[48] και σε κλωνοποιημένα βοοειδή.[49] Σπάνιες περιπτώσεις ανδρικής μιτοχονδριακής κληρονομικότητας έχουν καταγραφεί σε ανθρώπους.[50][51][52][53] Αν και πολλές από αυτές τις περιπτώσεις αφορούν κλωνοποιημένα έμβρυα ή επακόλουθη απόρριψη των πατρικών μιτοχονδρίων, άλλες τεκμηριώνουν την κληρονομικότητα και την επιμονή υπό εργαστηριακές συνθήκες.
Διπλή μονογονεϊκή κληρονομικότητα του mtDNA παρατηρείται σε δίθυρα μαλάκια. Σε αυτά τα είδη, τα θηλυκά έχουν μόνο έναν τύπο mtDNA (F), ενώ τα αρσενικά έχουν mtDNA τύπου F στα σωματικά τους κύτταρα, αλλά M τύπο mtDNA (που μπορεί να αποκλίνουν έως και 30%) σε κύτταρα βλαστικής σειράς.[54] Μιτοχόνδρια που έχουν κληρονομηθεί από πατέρα έχουν επίσης αναφερθεί σε ορισμένα έντομα όπως η δροσόφιλα [55][56] οι μέλισσες [57] και περιοδικά τζιτζίκια.[58]
Μιτοχονδριακή δωρεά Επεξεργασία
Μια τεχνική εξωσωματικής γονιμοποίησης (IVF) γνωστή ως μιτοχονδριακή δωρεά ή θεραπεία μιτοχονδριακής υποκατάστασης (mitochondrial replacement therapy (MRT)) οδηγεί σε απογόνους που περιέχουν mtDNA από δότρια και πυρηνικό DNA από μητέρα και πατέρα. Στη διαδικασία μεταφοράς ατράκτου, ο πυρήνας ενός ωαρίου εισάγεται στο κυτταρόπλασμα ενός ωαρίου από μια γυναίκα δότη στην οποία έχει αφαιρεθεί ο πυρήνας του, αλλά εξακολουθεί να περιέχει το mtDNA της γυναίκας του δότη. Το σύνθετο ωάριο γονιμοποιείται στη συνέχεια με το σπέρμα του άνδρα. Η διαδικασία χρησιμοποιείται όταν μια γυναίκα με γενετικά ελαττωματικά μιτοχόνδρια επιθυμεί να προδημιουργήσει και να γεννήσει απογόνους με υγιή μιτοχόνδρια. [59] Το πρώτο γνωστό παιδί που γεννήθηκε ως αποτέλεσμα δωρεάς μιτοχονδρίων ήταν ένα αγόρι που γεννήθηκε από ένα ζευγάρι της Ιορδανίας στο Μεξικό στις 6 Απριλίου 2016. [60]
Μεταλλάξεις και ασθένειες Επεξεργασία
Ευαισθησία Επεξεργασία
Η έννοια ότι το mtDNA είναι ιδιαίτερα ευαίσθητο σε δραστικές μορφές οξυγόνου που δημιουργούνται από την αναπνευστική αλυσίδα λόγω της εγγύτητάς του παραμένει αμφιλεγόμενη.[61] Το mtDNA δεν συσσωρεύει περισσότερο οξειδωτική βλάβη βάσης από το πυρηνικό DNA. [62] Έχει αναφερθεί ότι τουλάχιστον ορισμένοι τύποι οξειδωτικής βλάβης του DNA επιδιορθώνονται πιο αποτελεσματικά στα μιτοχόνδρια από ό, τι στον πυρήνα. [63] Το mtDNA είναι συσκευασμένο με πρωτεΐνες που φαίνεται να είναι εξίσου προστατευτικές με τις πρωτεΐνες της πυρηνικής χρωματίνης.[64] Επιπλέον, τα μιτοχόνδρια ανέπτυξαν έναν μοναδικό μηχανισμό που διατηρεί την ακεραιότητα του mtDNA μέσω της υποβάθμισης υπερβολικά κατεστραμμένων γονιδιωμάτων που ακολουθείται από αναπαραγωγή άθικτου/επιδιορθωμένου mtDNA. Αυτός ο μηχανισμός δεν υπάρχει στον πυρήνα και ενεργοποιείται από πολλαπλά αντίγραφα mtDNA που υπάρχουν στα μιτοχόνδρια. [65]Το αποτέλεσμα της μετάλλαξης στο mtDNA μπορεί να είναι μια αλλαγή στις οδηγίες κωδικοποίησης για ορισμένες πρωτεΐνες, [66] που μπορεί να έχουν επίδραση στο μεταβολισμό του οργανισμού ή/και στην φυσική κατάσταση.
Γενετικές ασθένειες Επεξεργασία
Οι μεταλλάξεις του μιτοχονδριακού DNA μπορούν να οδηγήσουν σε διάφορες ασθένειες όπως δυσανεξία στην άσκηση και το σύνδρομο Kearns – Sayre (KSS), οι οποίες αναγκάζουν ένα άτομο να χάσει την πλήρη λειτουργία των κινήσεων της καρδιάς, των οφθαλμών και των μυών. Ορισμένα στοιχεία υποδηλώνουν ότι μπορεί να είναι σημαντικοί συντελεστές στη διαδικασία γήρανσης και σε παθολογίες που σχετίζονται με την ηλικία.[67] Ειδικότερα στο πλαίσιο της νόσου, η αναλογία των μεταλλαγμένων μορίων mtDNA σε ένα κύτταρο ονομάζεται ετεροπλασμία. Η κατανομή της ετεροπλασμίας εντός και μεταξύ κυττάρων υπαγορεύει την έναρξη και τη σοβαρότητα της νόσου[68] και επηρεάζονται από περίπλοκες στοχαστικές διαδικασίες εντός του κυττάρου και κατά τη διάρκεια της ανάπτυξης.[27][69]
Οι μεταλλάξεις στα μιτοχονδριακά tRNAs μπορεί να ευθύνονται για σοβαρές ασθένειες όπως τα σύνδρομα MELAS και MERRF.[70]
Οι μεταλλάξεις στα πυρηνικά γονίδια που κωδικοποιούν πρωτεΐνες που χρησιμοποιούν τα μιτοχόνδρια μπορούν επίσης να συμβάλουν σε μιτοχονδριακά νοσήματα. Αυτές οι ασθένειες δεν ακολουθούν μιτοχονδριακά πρότυπα κληρονομικότητας, αλλά αντίθετα ακολουθούν τα Μεντελιανά πρότυπα κληρονομικότητας.[71]
Χρήση στη διάγνωση ασθενειών Επεξεργασία
Πρόσφατα χρησιμοποιήθηκε μια μετάλλαξη στο mtDNA για να βοηθήσει στη διάγνωση του καρκίνου του προστάτη σε ασθενείς με αρνητική βιοψία του προστάτη.[72][73]Μεταβολές mtDNA μπορούν να ανιχνευθούν στα βιορευστά ασθενών με καρκίνο.[74]
Σχέση με τη γήρανση Επεξεργασία
Αν και η ιδέα είναι αμφιλεγόμενη, ορισμένα στοιχεία υποδηλώνουν μια σχέση μεταξύ της γήρανσης και της δυσλειτουργίας του μιτοχονδριακού γονιδιώματος.[75] Ουσιαστικά, οι μεταλλάξεις στο mtDNA διαταράσσουν μια προσεκτική ισορροπία παραγωγής δραστικών μορφών οξυγόνου (ROS) και ενζυμικής απομάκρυνσης ROS (από ένζυμα όπως σουπεροξειδική δισμουτάση, καταλάση, υπεροξειδάση γλουταθειόνης (glutathione peroxidase) και άλλα). Ωστόσο, ορισμένες μεταλλάξεις που αυξάνουν την παραγωγή ROS (π.χ., μειώνοντας την αντιοξειδωτική άμυνα) στα σκουλήκια αυξάνουν, αντί να μειώνουν, τη μακροζωία τους.[61] Επίσης, οι γυμνοί τυφλοπόντικες (Naked mole-rat), τρωκτικά περίπου στο μέγεθος των ποντικιών, ζουν περίπου οκτώ φορές περισσότερο από τα ποντίκια παρά το γεγονός ότι έχουν μειώσει, σε σύγκριση με τα ποντίκια, την αντιοξειδωτική άμυνα και εχουν αυξημένη οξειδωτική βλάβη στα βιομόρια.[76] Κάποτε, θεωρήθηκε ότι υπήρχε ένας θετικός βρόχος ανατροφοδότησης στην εργασία (ένας 'φαύλος κύκλος'), καθώς το μιτοχονδριακό DNA συσσωρεύει γενετική βλάβη που προκαλείται από τις ελεύθερες ρίζες, τα μιτοχόνδρια χάνουν τη λειτουργία τους και διαρρέουν τις ελεύθερες ρίζες στο κυτοσόλιο. Η μείωση της μιτοχονδριακής λειτουργίας μειώνει τη συνολική μεταβολική απόδοση. [77] Ωστόσο, αυτή η έννοια διαψεύστηκε οριστικά όταν αποδείχθηκε ότι τα ποντίκια, τα οποία τροποποιήθηκαν γενετικά για να συσσωρεύουν μεταλλάξεις mtDNA με επιταχυνόμενο ρυθμό γερνούν πρόωρα, αλλά οι ιστοί τους δεν παράγουν περισσότερο ROS όπως προβλέπεται από την υπόθεση του 'φαύλου κύκλου'.[78] Υποστηρίζοντας μια σχέση μεταξύ μακροζωίας και μιτοχονδριακού DNA, ορισμένες μελέτες έχουν βρει συσχετίσεις μεταξύ βιοχημικών ιδιοτήτων του μιτοχονδριακού DNA και της μακροζωίας των ειδών. [79] Διεξάγεται εκτεταμένη έρευνα για περαιτέρω διερεύνηση αυτού του συνδέσμου και μεθόδων για την καταπολέμηση της γήρανσης. Επί του παρόντος, η γονιδιακή θεραπεία και η διατροφική συμπλήρωση είναι δημοφιλείς τομείς εξελισσόμενης έρευνας.[80][81] Ο Bjelakovic κ.α. ανέλυσαν τα αποτελέσματα 78 μελετών μεταξύ 1977 και 2012, που περιελάμβαναν συνολικά 296.707 συμμετέχοντες και συμπέραναν ότι τα αντιοξειδωτικά συμπληρώματα δεν μειώνουν τη θνησιμότητα από όλες τις αιτίες, ούτε παρατείνουν τη διάρκεια ζωής, ενώ μερικά από αυτά, όπως βήτα καροτίνη, βιταμίνη Ε και υψηλότερες δόσεις βιταμίνης Α, μπορούν στην πραγματικότητα να αυξήσουν τη θνησιμότητα.[82]
Νευροεκφυλιστικές ασθένειες Επεξεργασία
Αυξημένη βλάβη του του mtDNA είναι χαρακτηριστικό πολλών νευροεκφυλιστικών ασθενειών.
Οι εγκέφαλοι ατόμων με νόσο του Αλτσχάιμερ έχουν αυξημένα επίπεδα οξειδωτικής βλάβης στο DNA τόσο στο πυρηνικό DNA όσο και στο mtDNA, αλλά το mtDNA έχει περίπου 10 φορές υψηλότερα επίπεδα από το πυρηνικό DNA.[83] Έχει προταθεί ότι η γήρανση στα μιτοχόνδρια είναι ο κρίσιμος παράγοντας στην προέλευση του νευροεκφυλισμού στη νόσο Αλτσχάιμερ.[84]
Στην νόσος του Χάντινγκτον, η μεταλλαγμένη πρωτεΐνη χαντινγκτίνη προκαλεί μιτοχονδριακή δυσλειτουργία που περιλαμβάνει αναστολή της μιτοχονδριακής μεταφοράς ηλεκτρονίων, υψηλότερα επίπεδα δραστικών μορφών οξυγόνου και αυξημένη οξειδωτική καταπόνηση.[85] Η μεταλλαγμένη πρωτεΐνη χαντινγκτίνη προάγει την οξειδωτική βλάβη στο mtDNA, καθώς και το πυρηνικό DNA, που μπορεί να συμβάλει στην παθολογία της νόσου του Χάντινγκτον.[86]
Το προϊόν οξείδωσης του DNA 8-οξογουανίνη (8- oxoG) είναι ένας καθιερωμένος δείκτης της οξειδωτικής βλάβης του DNA. Σε άτομα με αμυοτροφική πλευρική σκλήρυνση (ALS), τα ένζυμα που συνήθως επιδιορθώνουν βλάβες 8-oxoG στο mtDNA των σπονδυλικών κινητικών νευρώνων είναι εξασθενημένα.[87] Έτσι, η οξειδωτική βλάβη στο mtDNA των κινητικών νευρώνων μπορεί να είναι σημαντικός παράγοντας στην αιτιολογία της ALS.
Συσχέτιση της σύνθεσης βάσης mtDNA με διαστήματα ζωής ζώων Επεξεργασία
Κατά την τελευταία δεκαετία, μια ισραηλινή ερευνητική ομάδα με επικεφαλής τον καθηγητή Vadim Fraifeld έδειξε ότι υπάρχουν ισχυρές και σημαντικές συσχετίσεις μεταξύ της βασικής σύστασης του mtDNA και της μέγιστης διάρκειας ζωής για συγκεκριμένα είδη των ζώων.[88][89][90] Όπως αποδείχθηκε στη δουλειά τους, υψηλότερη περιεκτικότητα του mtDNA σε γουανίνη + κυτοσίνη (GC%) συνδέεται έντονα με μεγαλύτερη μέγιστη διάρκεια ζωής στα ζώα. Μια πρόσθετη παρατήρηση είναι ότι ο συσχετισμός GC% του mtDNA με τη μέγιστη διάρκεια ζωής είναι ανεξάρτητος από τη γνωστή συσχέτιση μεταξύ του μεταβολικού ρυθμού των ζωικών ειδών και της μέγιστης διάρκειας ζωής. Το GC% του mtDNA και ο μεταβολικός ρυθμός ανάπαυσης εξηγούν τις διαφορές στη μέγιστη διάρκεια ζωής των ζωικών ειδών με πολλαπλασιαστικό τρόπο (δηλαδή, μέγιστη διάρκεια ζωής των ειδών = ο μεταβολικός ρυθμός GC% * του mtDNA).[89] Για να υποστηριχθεί η επιστημονική κοινότητα στην εκτέλεση συγκριτικών αναλύσεων μεταξύ χαρακτηριστικών του mtDNA και μακροβιότητας στα ζώα, δημιουργήθηκε μια ειδική βάση δεδομένων με το όνομα MitoAge.[91]
Σχέση με μη Β (μη κανονικές) δομές DNA Επεξεργασία
Τα σημεία θραύσης απαλοιφής εμφανίζονται συχνά εντός ή κοντά σε περιοχές που δείχνουν μη κανονικές (μη Β) διαμορφώσεις, δηλαδή σε φουρκέτες, σταυροειδή και στοιχεία που μοιάζουν με τριφύλλι.[92] Επιπλέον, υπάρχουν δεδομένα που υποστηρίζουν τη συμμετοχή των εγγενώς καμπυλών περιοχών που στρεβλώνουν την έλικα και των μακρών G-τετράδων στην πρόκληση συμβάντων αστάθειας. Επιπλέον, υψηλότερες πυκνότητες σημείων θραύσης παρατηρήθηκαν σταθερά εντός των λοξών περιοχών GC και σε κοντινή απόσταση του εκφυλισμένου μοτίβου αλληλουχίας YMMYMNNMMHM.[93]
Χρήση στην ιατροδικαστική Επεξεργασία
Σε αντίθεση με το πυρηνικό DNA, το οποίο κληρονομείται και από τους δύο γονείς και στο οποίο τα γονίδια αναδιατάσσονται κατά τη διαδικασία του ανασυνδυασμού, συνήθως δεν υπάρχει αλλαγή στο mtDNA από γονέα σε απόγονο. Αν και το mtDNA ανασυνδυάζεται, το κάνει με αντίγραφα του εαυτού του μέσα στο ίδιο μιτοχόνδριο. Εξαιτίας αυτού και επειδή ο ρυθμός μετάλλαξης του mtDNA στα ζώα είναι υψηλότερος από αυτόν του πυρηνικού DNA,[94] το mtDNA είναι ένα ισχυρό εργαλείο για την παρακολούθηση των προγόνων μέσω των θηλυκών (μητρική γραμμή) και έχει χρησιμοποιηθεί σε αυτόν τον ρόλο για την παρακολούθηση της καταγωγής πολλών ειδών πριν από εκατοντάδες γενιές.
Ο γρήγορος ρυθμός μετάλλαξης (σε ζώα) καθιστά το mtDNA χρήσιμο για την εκτίμηση γενετικών σχέσεων ατόμων ή ομάδων μέσα σε ένα είδος και επίσης για τον προσδιορισμό και τον ποσοτικό προσδιορισμό της φυλογένεσης μεταξύ διαφορετικών ειδών. Για να γίνει αυτό, οι βιολόγοι προσδιορίζουν και στη συνέχεια συγκρίνουν τις αλληλουχίες mtDNA από διαφορετικά άτομα ή είδη. Τα δεδομένα από τις συγκρίσεις χρησιμοποιούνται για τη δημιουργία ενός δικτύου σχέσεων μεταξύ των αλληλουχιών, το οποίο παρέχει μια εκτίμηση των σχέσεων μεταξύ των ατόμων ή των ειδών από τα οποία λήφθηκαν τα mtDNA. Το mtDNA μπορεί να χρησιμοποιηθεί για την εκτίμηση της σχέσης τόσο των στενών συγγενικών όσο και εξ αποστάσεως συγγενικών ειδών. Λόγω του υψηλού ποσοστού μετάλλαξης του mtDNA σε ζώα, οι 3ες θέσεις των κωδικονίων αλλάζουν σχετικά γρήγορα, και έτσι παρέχουν πληροφορίες σχετικά με τις γενετικές αποστάσεις μεταξύ στενά συγγενικών ατόμων ή ειδών. Από την άλλη πλευρά, ο ρυθμός υποκατάστασης των μιτοχονδριακών πρωτεϊνών είναι πολύ χαμηλός, έτσι οι αλλαγές αμινοξέων συσσωρεύονται αργά (με αντίστοιχες αργές μεταβολές στις θέσεις 1ου και 2ου κωδικονίου) και έτσι παρέχουν πληροφορίες σχετικά με τις γενετικές αποστάσεις των μακρινών συγγενικών ειδών. Στατιστικά πρότυπα που αντιμετωπίζουν χωριστά τα ποσοστά υποκατάστασης μεταξύ των θέσεων κωδικονίου, μπορούν έτσι να χρησιμοποιηθούν για την ταυτόχρονη εκτίμηση φυλογενειών που περιέχουν στενά και μακρινά συγγενικά είδη[70]
Το μιτοχονδριακό DNA έγινε αποδεκτό για πρώτη φορά σε δικαστήριο των ΗΠΑ το 1996 κατά τη διάρκεια της δίκης της "Πολιτείας του Τένεσι κατά Paul Ware".[95]
Στην υπόθεση στις Ηνωμένες Πολιτείες του 1998 για της Πολιτείας της Πενσυλβάνια κατά της Patricia Lynne Rorrer,[96] το μιτοχονδριακό DNA έγινε δεκτό ως αποδεικτικό στοιχείο στην Πολιτεία της Πενσυλβάνια για πρώτη φορά.[97][98]
Το μιτοχονδριακό DNA εισήχθη για πρώτη φορά ως αποδεικτικό στοιχείο στην Καλιφόρνια των Ηνωμένων Πολιτειών, στην επιτυχή δίωξη του Ντέιβιντ Γουέστερφιλντ για την απαγωγή και δολοφονία του 7χρονου το 2002 Ντανιέλ βαν Νταμ στο Σαν Ντιέγκο: όπου χρησιμοποιήθηκε για την αναγνώριση τόσο ανθρώπου όσο και σκύλου.[99] Αυτή ήταν η πρώτη δίκη στις ΗΠΑ με αποδοχή DNA σκύλου.[100]
Τα λείψανα του Ριχάρδου Γ΄ της Αγγλίας, που πέθανε το 1485, ταυτοποιήθηκαν συγκρίνοντας το mtDNA του με εκείνο δύο μητρικών απογόνων της αδελφής του που ζούσαν το 2013, 527 χρόνια μετά τον θάνατό του. [101]
Χρήση στην εξελικτική και τη συστηματική βιολογία Επεξεργασία
Το mtDNA διατηρείται σε ολόκληρο τον ευκαρυωτικό οργανισμό δεδομένου του κρίσιμου ρόλου των μιτοχονδρίων στην κυτταρική αναπνοή. Ωστόσο, λόγω της λιγότερο αποτελεσματικής επιδιόρθωσης του DNA (σε σύγκριση με το πυρηνικό DNA) έχει σχετικά υψηλό ρυθμό μετάλλαξης (αλλά αργό σε σύγκριση με άλλες περιοχές του DNA, όπως μικροδορυφόροι), γεγονός που το καθιστά χρήσιμο για τη μελέτη των εξελικτικών σχέσεων - φυλογένεση - των οργανισμών. Οι βιολόγοι μπορούν να προσδιορίσουν και στη συνέχεια να συγκρίνουν αλληλουχίες mtDNA μεταξύ διαφορετικών ειδών και να χρησιμοποιήσουν τις συγκρίσεις για να δημιουργήσουν ένα εξελικτικό δέντρο για τα είδη που εξετάστηκαν.
Για παράδειγμα, ενώ τα περισσότερα πυρηνικά γονίδια είναι σχεδόν πανομοιότυπα μεταξύ ανθρώπων και χιμπαντζήδων, τα μιτοχονδριακά γονιδιώματά τους διαφέρουν κατά 9,8%. Τα μιτοχονδριακά γονιδιώματα του ανθρώπου και του δυτικού γορίλα είναι 11,8% διαφορετικά, υποδηλώνοντας ότι μπορεί να είμαστε περισσότερο παρόμοιοι με τους χιμπατζήδες από τους γορίλες.[102]
Ιστορικό Επεξεργασία
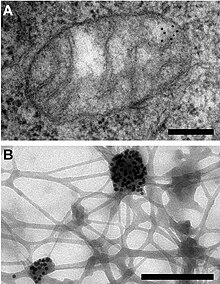
Το μιτοχονδριακό DNA ανακαλύφθηκε τη δεκαετία του 1960 από τους Margit M. K. Nass και Sylvan Nass με ηλεκτρονική μικροσκοπία ως ευαίσθητα σε DNase νήματα μέσα στα μιτοχόνδρια, [103] και από τους Ellen Haslbrunner, Hans Tuppy και Gottfried Schatz με βιοχημικές δοκιμασίες σε εξαιρετικά καθαρισμένα μιτοχονδριακά κλάσματα.[104]
Βάσεις δεδομένων μιτοχονδριακών Επεξεργασία
Αρκετές εξειδικευμένες βάσεις δεδομένων έχουν δημιουργηθεί που συλλέγουν αλληλουχίες μιτοχονδριακών γονιδιωμάτων καθώς και άλλες πληροφορίες. Αν ακαι οι περισσότερες βάσεις δεδομένων εστιάζονται σε δεδομένα αλληλουχίας, μερικές από αυτές περιλαμβάνουν φυλογενετικές ή λειτουργικές πληροφορίες.
- AmtDB: μια βάση δεδομένων των αρχαίων ανθρωπίνων μιτοχονδριακών γονιδιωμάτωνa.[105]
- InterMitoBase: μια βάση δεδομένων με σχόλια και ανάλυση των αλληλεπιδράσεων πρωτεϊνών-πρωτεϊνών για τα ανθρώπινα μιτοχόνδρια. [106] (προφανώς ενημερώθηκε, αλλά εξακολουθεί να είναι διαθέσιμη)
- MitoBreak: η βάση δεδομένων των σημείων θραύσης του μιτοχονδριακού DNA.[107]
- MitoFish και MitoAnnotator: μια βάση δεδομένων μιτοχονδριακών γονιδιωμάτων ιχθύων. [108] Δείτε επίσης Cawthorn κ.α.[109]
- Mitome: μια βάση δεδομένων για συγκριτικά μιτοχονδριακά γονιδιώματα στα μετάζωα. [110] (δεν είναι πια διαθέσιμη)
- MitoRes: μια πηγή μιτοχονδριακών γονιδιωμάτων πυρηνικά κωδικοποιημένων καθώς και των προϊόντων τους στα μετάζωα[111] (προφανώς δεν ενημερώνεται πια)
- MitoSatPlant: βάση δεδομένων μιτοχονδριακών μικροδορυφόρων των πράσινων φυτών.[112]
- MitoZoa 2.0: μια βάση δεδομένων για συγκριτικές και εξελικτικές αναλύσεις των μιτοχονδριακών γονιδιωμάτων σε μετάζωα.[113] (δεν είναι πια διαθέσιμη)
Βάσεις δεδομένων συσχετισμού MtDNA-φαινοτύπου Επεξεργασία
Μελέτες συσχέτισης σε ολόκληρο το γονιδίωμα μπορούν να αποκαλύψουν συσχετίσεις των γονιδίων του mtDNA και των μεταλλάξεων τους με τους φαινότυπους συμπεριλαμβανομένης της διάρκεια ζωής και των κινδύνων ασθενειών. Το 2021, η μεγαλύτερη, με βάση τη UK Biobank, μελέτη συσχέτισης του γονιδιώματος και του μιτοχονδριακού DNA αποκάλυψε 260 νέες συσχετίσεις με φαινότυπους, συμπεριλαμβανομένων της διάρκειας ζωής και των κινδύνων ασθενειών όπως π.χ.. διαβήτης τύπου 2. [114][115]
Βάσεις δεδομένων μιτοχονδριακών μεταλλάξεων Επεξεργασία
Υπάρχουν αρκετές εξειδικευμένες βάσεις δεδομένων που αναφέρουν πολυμορφισμούς και μεταλλάξεις στο ανθρώπινο μιτοχονδριακό DNA, μαζί με την εκτίμηση της παθογένειας τους.
Παραπομπές Επεξεργασία
- ↑ «Powerhouse of the cell». Scientific American 197 (1): 131–40. 1957. doi:. Bibcode: 1957SciAm.197a.131S. https://archive.org/details/sim_scientific-american_1957-07_197_1/page/131.
- ↑ «The functional organization of mitochondrial genomes in human cells». BMC Biology 2: 9. May 2004. doi:. PMID 15157274.
- ↑ Sykes B (10 Σεπτεμβρίου 2003). «Mitochondrial DNA and human history». The Human Genome. Wellcome Trust. Αρχειοθετήθηκε από το πρωτότυπο στις 7 Σεπτεμβρίου 2015. Ανακτήθηκε στις 5 Φεβρουαρίου 2012.
- ↑ Anderson S, Bankier AT, Barrell BG, de Bruijn MH, Coulson AR, Drouin J, Eperon IC, Nierlich DP, Roe BA, Sanger F, Schreier PH, Smith AJ, Staden R, Young IG. (1981). «Sequence and organization of the human mitochondrial genome.». Nature 290 (5806): 457–65. doi:. PMID 7219534. Bibcode: 1981Natur.290..457A.
- ↑ «[Not Available»]. Génétique, Sélection, Évolution 18 (1): 73–98. 1986-01-01. doi:. PMID 22879234.
- ↑ «Molecular systematics of armadillos (Xenarthra, Dasypodidae): contribution of maximum likelihood and Bayesian analyses of mitochondrial and nuclear genes». Molecular Phylogenetics and Evolution 28 (2): 261–75. August 2003. doi:. PMID 12878463. https://hal.archives-ouvertes.fr/halsde-00192983.
- ↑ «Combining multiple autosomal introns for studying shallow phylogeny and taxonomy of Laurasiatherian mammals: Application to the tribe Bovini (Cetartiodactyla, Bovidae)». Molecular Phylogenetics and Evolution 66 (3): 766–75. March 2013. doi:. PMID 23159894.
- ↑ 8,0 8,1 8,2 «Evolutionary Inference across Eukaryotes Identifies Specific Pressures Favoring Mitochondrial Gene Retention». Cell Systems 2 (2): 101–11. February 2016. doi:. PMID 27135164.
- ↑ van der Giezen, Mark· Tovar, Jorge· Clark, C. Graham (2005). «Mitochondrion‐Derived Organelles in Protists and Fungi». A Survey of Cell Biology. International Review of Cytology. 244. σελίδες 175–225. doi:10.1016/S0074-7696(05)44005-X. ISBN 978-0-12-364648-4. PMID 16157181.
- ↑ «Evolution of mitochondrial gene content: gene loss and transfer to the nucleus». Molecular Phylogenetics and Evolution 29 (3): 380–95. December 2003. doi:. PMID 14615181.
- ↑ «Mitochondrial genomes are retained by selective constraints on protein targeting». Proceedings of the National Academy of Sciences of the United States of America 112 (33): 10154–61. August 2015. doi:. PMID 26195779. Bibcode: 2015PNAS..11210154B.
- ↑ «Why chloroplasts and mitochondria retain their own genomes and genetic systems: Colocation for redox regulation of gene expression». Proceedings of the National Academy of Sciences of the United States of America 112 (33): 10231–8. August 2015. doi:. PMID 26286985. Bibcode: 2015PNAS..11210231A.
- ↑ 13,0 13,1 «Diversity of mitochondrial genome organization». Biochemistry. Biokhimiia 77 (13): 1424–35. December 2012. doi:. PMID 23379519.
- ↑ «Linear mitochondrial genomes: 30 years down the line». Trends in Genetics 14 (5): 184–8. May 1998. doi:. PMID 9613202. https://archive.org/details/sim_trends-in-genetics_1998-05_14_5/page/184.
- ↑ Lavrov, Dennis V.; Pett, Walker (2016-09-26). «Animal Mitochondrial DNA as We Do Not Know It: mt-Genome Organization and Evolution in Nonbilaterian Lineages». Genome Biology and Evolution 8 (9): 2896–2913. doi:. ISSN 1759-6653. PMID 27557826. PMC 5633667. https://pubmed.ncbi.nlm.nih.gov/27557826.
- ↑ Stampar, Sérgio N.; Broe, Michael B.; Macrander, Jason; Reitzel, Adam M.; Brugler, Mercer R.; Daly, Marymegan (2019-04-15). «Linear Mitochondrial Genome in Anthozoa (Cnidaria): A Case Study in Ceriantharia». Scientific Reports 9 (1): 6094. doi:. ISSN 2045-2322. PMID 30988357. Bibcode: 2019NatSR...9.6094S.
- ↑ Yahalomi, Dayana; Atkinson, Stephen D.; Neuhof, Moran; Chang, E. Sally; Philippe, Hervé; Cartwright, Paulyn; Bartholomew, Jerri L.; Huchon, Dorothée (10 March 2020). «A cnidarian parasite of salmon (Myxozoa: Henneguya) lacks a mitochondrial genome». Proceedings of the National Academy of Sciences 117 (10): 5358–5363. doi:. PMID 32094163.
- ↑ Starr, Michelle. «Scientists Find The First-Ever Animal That Doesn't Need Oxygen to Survive». ScienceAlert (στα Αγγλικά). Ανακτήθηκε στις 25 Φεβρουαρίου 2020.
- ↑ «Rapid evolution of enormous, multichromosomal genomes in flowering plant mitochondria with exceptionally high mutation rates». PLOS Biology 10 (1): e1001241. January 2012. doi:. PMID 22272183.
- ↑ «The mitochondrial genome is large and variable in a family of plants (cucurbitaceae)». Cell 25 (3): 793–803. September 1981. doi:. PMID 6269758.
- ↑ «Origins and recombination of the bacterial-sized multichromosomal mitochondrial genome of cucumber». The Plant Cell 23 (7): 2499–513. July 2011. doi:. PMID 21742987.
- ↑ «Mitochondrial DNA (mtDNA)» (PDF). Integrated DNA Technologies. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 29 Ιουλίου 2016. Ανακτήθηκε στις 25 Φεβρουαρίου 2016.
- ↑ «Whole mitochondrial genome sequence of an Indian Plasmodium falciparum field isolate» (στα αγγλικά). The Korean Journal of Parasitology 52 (1): 99–103. February 2014. doi:. PMID 24623891.
- ↑ «Functional human mitochondrial DNA polymerase gamma forms a heterotrimer». The Journal of Biological Chemistry 281 (1): 374–82. January 2006. doi:. PMID 16263719.
- ↑ «The mitochondrial DNA helicase TWINKLE can assemble on a closed circular template and support initiation of DNA synthesis». Nucleic Acids Research 39 (21): 9238–49. November 2011. doi:. PMID 21840902.
- ↑ 26,0 26,1 26,2 «Mitochondrial DNA transmission, replication and inheritance: a journey from the gamete through the embryo and into offspring and embryonic stem cells». Human Reproduction Update 16 (5): 488–509. 2010. doi:. PMID 20231166.
- ↑ 27,0 27,1 27,2 «Stochastic modelling, Bayesian inference, and new in vivo measurements elucidate the debated mtDNA bottleneck mechanism». eLife 4: e07464. June 2015. doi:. PMID 26035426.
- ↑ 28,0 28,1 28,2 «Mitochondrial DNA Transcription and Its Regulation: An Evolutionary Perspective.». Trends Genet 34 (9): 682–692. 2018. doi:. PMID 29945721.
- ↑ Barchiesi A, Vascotto C (2019). «Transcription, Processing, and Decay of Mitochondrial RNA in Health and Disease.». Int J Mol Sci 20 (9): 2221. doi:. PMID 31064115.
- ↑ Μιτοχόνδριο του "Homo sapiens", πλήρες γονιδίωμα "Revised Cambridge Reference Sequence (rCRS): accession NC_012920", National Center for Biotechnology Information. Retrieved on 20 February 2017.
- ↑ «DNA replication and transcription in mammalian mitochondria». Annual Review of Biochemistry 76 (1): 679–99. 2007-06-19. doi:. PMID 17408359.
- ↑ «Mitochondrial Transcription of Entomopathogenic Fungi Reveals Evolutionary Aspects of Mitogenomes». Frontiers in Microbiology 13 (821638). 21 March 2022. doi:. PMID 35387072.
- ↑ «tRNA punctuation model of RNA processing in human mitochondria». Nature 290 (5806): 470–4. April 1981. doi:. PMID 7219536. Bibcode: 1981Natur.290..470O.
- ↑ 34,0 34,1 34,2 34,3 «Mitochondrial-genome-encoded RNAs: differential regulation by corticotropin in bovine adrenocortical cells». Proceedings of the National Academy of Sciences of the United States of America 90 (22): 10509–13. Nov 1993. doi:. PMID 7504267. Bibcode: 1993PNAS...9010509R.
- ↑ «Lost in the zygote: the dilution of paternal mtDNA upon fertilization». Heredity 101 (5): 429–34. November 2008. doi:. PMID 18685570.
- ↑ «Influence of microsurgical varicocelectomy on human sperm mitochondrial DNA copy number: a pilot study». Journal of Assisted Reproduction and Genetics 29 (8): 759–64. August 2012. doi:. PMID 22562241.
- ↑ «Biparental Inheritance of Mitochondrial DNA in Humans». Proceedings of the National Academy of Sciences of the United States of America 115 (51): 13039–13044. December 2018. doi:. PMID 30478036.
- ↑ «Ubiquitin tag for sperm mitochondria». Nature 402 (6760): 371–2. November 1999. doi:. PMID 10586873. Bibcode: 1999Natur.402..371S. Discussed in: Travis, John (2000). «Mom's Eggs Execute Dad's Mitochondria». Science News 157 (1): 5. doi:. https://www.sciencenews.org/article/moms-eggs-execute-dads-mitochondria.
- ↑ «Hiring a DNA Testing Company Genealogy». Family Search. The Church of Jesus Christ of Latter-day Saints. 2016. Ανακτήθηκε στις 2 Οκτωβρίου 2016.
- ↑ «Multiple and ancient origins of the domestic dog». Science 276 (5319): 1687–9. June 1997. doi:. PMID 9180076.
- ↑ «The strength and timing of the mitochondrial bottleneck in salmon suggests a conserved mechanism in vertebrates». PLOS ONE 6 (5): e20522. 2011. doi:. PMID 21655224. Bibcode: 2011PLoSO...620522W.
- ↑ «A reduction of mitochondrial DNA molecules during embryogenesis explains the rapid segregation of genotypes». Nature Genetics 40 (2): 249–54. February 2008. doi:. PMID 18223651.
- ↑ «The mitochondrial bottleneck occurs without reduction of mtDNA content in female mouse germ cells». Nature Genetics 39 (3): 386–90. March 2007. doi:. PMID 17293866.
- ↑ «The mitochondrial DNA genetic bottleneck results from replication of a subpopulation of genomes». Nature Genetics 40 (12): 1484–8. December 2008. doi:. PMID 19029901.
- ↑ «Mitogenomic analysis of a 50-generation chicken pedigree reveals a rapid rate of mitochondrial evolution and evidence for paternal mtDNA inheritance». Biology Letters 11 (10): 20150561. October 2015. doi:. PMID 26510672.
- ↑ «Paternal inheritance of mitochondrial DNA in mice». Nature 352 (6332): 255–7. July 1991. doi:. PMID 1857422. Bibcode: 1991Natur.352..255G.
- ↑ «Maternal inheritance of mouse mtDNA in interspecific hybrids: segregation of the leaked paternal mtDNA followed by the prevention of subsequent paternal leakage». Genetics 148 (2): 851–7. February 1998. PMID 9504930. PMC 1459812. http://www.genetics.org/cgi/pmidlookup?view=long&pmid=9504930.
- ↑ «Further evidence for paternal inheritance of mitochondrial DNA in the sheep (Ovis aries)». Heredity 93 (4): 399–403. October 2004. doi:. PMID 15266295. https://archive.org/details/sim_heredity_2004-10_93_4/page/n82.
- ↑ «Composition of parental mitochondrial DNA in cloned bovine embryos». FEBS Letters 426 (3): 352–6. April 1998. doi:. PMID 9600265.
- ↑ «A105 Family Decoded: Discovery of Genome-Wide Fingerprints for Personalized Genomic Medicine». ScienceMED 3 (2): 115–126. April 2012.
- ↑ «Customized Biomedical Informatics». BMC Big Data Analytics 3. May 2018. doi:.
- ↑ «Paternal inheritance of mitochondrial DNA». The New England Journal of Medicine 347 (8): 576–80. August 2002. doi:. PMID 12192017.
- ↑ «Biparental Inheritance of Mitochondrial DNA in Humans». Proceedings of the National Academy of Sciences of the United States of America 115 (51): 13039–13044. December 2018. doi:. PMID 30478036.
- ↑ «Doubly uniparental inheritance: two mitochondrial genomes, one precious model for organelle DNA inheritance and evolution». DNA and Cell Biology 28 (2): 79–89. February 2009. doi:. PMID 19196051.
- ↑ «Further observation of paternal transmission of Drosophila mitochondrial DNA by PCR selective amplification method». Genetical Research 59 (2): 81–4. April 1992. doi:. PMID 1628820.
- ↑ «Paternal transmission of mitochondrial DNA as an integral part of mitochondrial inheritance in metapopulations of Drosophila simulans». Heredity 110 (1): 57–62. January 2013. doi:. PMID 23010820. PMC 3522233. https://archive.org/details/sim_heredity_2013-01_110_1/page/57.
- ↑ «Transfer of paternal mitochondrial DNA during fertilization of honeybee (Apis mellifera L.) eggs». Current Genetics 24 (6): 539–43. December 1993. doi:. PMID 8299176. https://archive.org/details/sim_current-genetics_1993-12_24_6/page/539.
- ↑ «Evidence for paternal leakage in hybrid periodical cicadas (Hemiptera: Magicicada spp.)». PLOS ONE 2 (9): e892. September 2007. doi:. PMID 17849021. Bibcode: 2007PLoSO...2..892F.
- ↑ Frith, Maxine (14 October 2003). «Ban on scientists trying to create three-parent baby». The Independent. https://www.independent.co.uk/news/science/ban-on-scientists-trying-to-create-threeparent-baby-583284.html.[νεκρός σύνδεσμος]
- ↑ Roberts, Michelle (2016-09-27). «First 'three person baby' born using new method» (στα αγγλικά). BBC News. https://www.bbc.co.uk/news/health-37485263. Ανακτήθηκε στις 2016-09-28.
- ↑ 61,0 61,1 «Is there more to aging than mitochondrial DNA and reactive oxygen species?». The FEBS Journal 276 (20): 5768–87. October 2009. doi:. PMID 19796285.
- ↑ «Mitochondrial endogenous oxidative damage has been overestimated». FASEB Journal 14 (2): 355–60. February 2000. doi:. PMID 10657991. https://archive.org/details/sim_faseb-journal_2000-02_14_2/page/355.
- ↑ «Repair of 8-oxoG is slower in endogenous nuclear genes than in mitochondrial DNA and is without strand bias». DNA Repair 1 (4): 261–73. April 2002. doi:. PMID 12509245. https://zenodo.org/record/1260266.
- ↑ «[Proteins associated with mitochondrial DNA protect it against the action of X-rays and hydrogen peroxide]» (στα ru). Biofizika 51 (4): 692–7. 2006. PMID 16909848.
- ↑ «The maintenance of mitochondrial DNA integrity--critical analysis and update». Cold Spring Harbor Perspectives in Biology 5 (5): a012641. May 2013. doi:. PMID 23637283.
- ↑ Hogan, C. Michael (2010). «Mutation». Στο: Monosson, E.· Cleveland, C. J. Encyclopedia of Earth. Washington DC: National Council for Science and the Environment.
- ↑ «Mitochondrial DNA and aging». Clinical Science 107 (4): 355–64. October 2004. doi:. PMID 15279618. https://semanticscholar.org/paper/c52e27abb1cf6e2d1b5690da425435216da78aab.
- ↑ «Mitochondrial DNA disease and developmental implications for reproductive strategies». Molecular Human Reproduction 21 (1): 11–22. January 2015. doi:. PMID 25425607.
- ↑ «MtDNA segregation in heteroplasmic tissues is common in vivo and modulated by haplotype differences and developmental stage». Cell Reports 7 (6): 2031–2041. June 2014. doi:. PMID 24910436.
- ↑ 70,0 70,1 «Mitochondrial DNA mutations in human disease». Nature Reviews Genetics 6 (5): 389–402. May 2005. doi:. PMID 15861210.
- ↑ «Mitochondrial disorders of the nuclear genome». Acta Myologica 28 (1): 16–23. July 2009. PMID 19772191.
- ↑ «3.4 kb mitochondrial genome deletion serves as a surrogate predictive biomarker for prostate cancer in histopathologically benign biopsy cores». Canadian Urological Association Journal 4 (5): E118-22. October 2010. doi:. PMID 20944788.
- ↑ «Accurate prediction of repeat prostate biopsy outcomes by a mitochondrial DNA deletion assay». Prostate Cancer and Prostatic Diseases 13 (2): 126–31. June 2010. doi:. PMID 20084081.
- ↑ Mair, R (2019). «Measurement of plasma cell-free mitochondrial tumor DNA improves detection of glioblastoma in patient-derived orthotopic xenograft models.». Cancer Research 79 (1): 220–230. doi:. PMID 30389699. PMC 6753020. https://www.repository.cam.ac.uk/handle/1810/286401.
- ↑ de Grey, Aubrey (1999). The Mitochondrial Free Radical Theory of Aging (PDF). ISBN 978-1-57059-564-6. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 3 Ιουνίου 2016. Ανακτήθηκε στις 18 Αυγούστου 2021.[Χρειάζεται σελίδα]
- ↑ «The naked mole-rat response to oxidative stress: just deal with it». Antioxidants & Redox Signaling 19 (12): 1388–99. October 2013. doi:. PMID 23025341.
- ↑ «Oxidative damage and mitochondrial decay in aging». Proceedings of the National Academy of Sciences of the United States of America 91 (23): 10771–8. November 1994. doi:. PMID 7971961. Bibcode: 1994PNAS...9110771S.
- ↑ «Somatic mtDNA mutations cause aging phenotypes without affecting reactive oxygen species production». Proceedings of the National Academy of Sciences of the United States of America 102 (50): 17993–8. December 2005. doi:. PMID 16332961. Bibcode: 2005PNAS..10217993T.
- ↑ «Mitochondrially encoded methionine is inversely related to longevity in mammals». Aging Cell 10 (2): 198–207. April 2011. doi:. PMID 21108730.
- ↑ «Functional foods, herbs and nutraceuticals: towards biochemical mechanisms of healthy aging». Biogerontology 5 (5): 275–89. 2004. doi:. PMID 15547316.
- ↑ «Gene therapy for the treatment of mitochondrial DNA disorders». Expert Opinion on Biological Therapy 5 (2): 183–94. February 2005. doi:. PMID 15757380.
- ↑ «Antioxidant supplements to prevent mortality». JAMA 310 (11): 1178–9. September 2013. doi:. PMID 24045742.
- ↑ «Increased oxidative damage in nuclear and mitochondrial DNA in Alzheimer's disease». Journal of Neurochemistry 93 (4): 953–62. May 2005. doi:. PMID 15857398.
- ↑ «Neuronal failure in Alzheimer's disease: a view through the oxidative stress looking-glass». Neuroscience Bulletin 30 (2): 243–52. April 2014. doi:. PMID 24733654.
- ↑ «Oxidative Stress in Neurodegenerative Diseases: From Molecular Mechanisms to Clinical Applications». Oxidative Medicine and Cellular Longevity 2017: 2525967. 2017. doi:. PMID 28785371.
- ↑ «Role of oxidative DNA damage in mitochondrial dysfunction and Huntington's disease pathogenesis». Free Radical Biology & Medicine 62: 102–110. September 2013. doi:. PMID 23602907.
- ↑ «Impairment of mitochondrial DNA repair enzymes against accumulation of 8-oxo-guanine in the spinal motor neurons of amyotrophic lateral sclerosis». Acta Neuropathologica 103 (4): 408–14. April 2002. doi:. PMID 11904761.
- ↑ «Mitochondrial genome anatomy and species-specific lifespan». Rejuvenation Research 9 (2): 223–6. 2006. doi:. PMID 16706648.
- ↑ 89,0 89,1 «Do mitochondrial DNA and metabolic rate complement each other in determination of the mammalian maximum longevity?». Rejuvenation Research 11 (2): 409–17. April 2008. doi:. PMID 18442324.
- ↑ «Telomere length and body temperature-independent determinants of mammalian longevity?». Frontiers in Genetics 4 (111): 111. 2013. doi:. PMID 23781235.
- ↑ «MitoAge: a database for comparative analysis of mitochondrial DNA, with a special focus on animal longevity». Nucleic Acids Research 44 (D1): D1262-5. January 2016. doi:. PMID 26590258.
- ↑ «Mitochondrial DNA deletions are associated with non-B DNA conformations». Nucleic Acids Research 40 (16): 7606–21. September 2012. doi:. PMID 22661583.
- ↑ «An appraisal of human mitochondrial DNA instability: new insights into the role of non-canonical DNA structures and sequence motifs». PLOS ONE 8 (3): e59907. 2013. doi:. PMID 23555828. Bibcode: 2013PLoSO...859907O.
- ↑ «Rapid evolution of animal mitochondrial DNA». Proceedings of the National Academy of Sciences of the United States of America 76 (4): 1967–71. April 1979. doi:. PMID 109836. Bibcode: 1979PNAS...76.1967B.
- ↑ Davis, C. Leland (1998). «Mitochondrial DNA: State of Tennessee v. Paul Ware». Profiles in DNA 1 (3): 6–7. http://www.promega.ca/~/media/files/resources/profiles%20in%20dna/103/mitochondrial%20dna%20state%20of%20tennessee%20v%20paul%20ware.pdf.
- ↑ [1] Court case name listed in the appeal.[απαιτείται πλήρης παραπομπή] Retrieved 17 April 2015.
- ↑ [2] Αρχειοθετήθηκε 2015-05-17 στο Wayback Machine.[αυτοδημοσιευμένη πηγή ;] Defense lawyer. Retrieved 17 April 2015.
- ↑ Garlicki, Debbie (11 March 1998). «DNA Tests Got Rorrer Life in Jail». The Morning Call.
- ↑ "Judge allows DNA in Samantha Runnion case," Associated Press, 18 February 2005. Retrieved 4 April 2007.
- ↑ "Canine DNA Admitted In California Murder Case," Αρχειοθετήθηκε 2 February 2014 στο Wayback Machine. Pit Bulletin Legal News, 5 December 2013. Retrieved 21 January 2014.
- ↑ Kennedy, Maev (4 February 2013). «Richard III: DNA confirms twisted bones belong to king». The Guardian. https://www.theguardian.com/science/2013/feb/04/richard-iii-dna-bones-king. Ανακτήθηκε στις 7 December 2014.
- ↑ Xu, X.; Arnason, U. (1996-05-01). «A complete sequence of the mitochondrial genome of the western lowland gorilla.» (στα αγγλικά). Molecular Biology and Evolution 13 (5): 691–698. doi:. ISSN 0737-4038. PMID 8676744. https://academic.oup.com/mbe/article/13/5/691/1083040.
- ↑ «INTRAMITOCHONDRIAL FIBERS WITH DNA CHARACTERISTICS: I. Fixation and Electron Staining Reactions». The Journal of Cell Biology 19 (3): 593–611. December 1963. doi:. PMID 14086138. PMC 2106331. https://archive.org/details/sim_journal-of-cell-biology_1963-12_19_3/page/593.
- ↑ «Deoxyribonucleic acid associated with yeast mitochondria». Biochemical and Biophysical Research Communications 15 (2): 127–32. March 1964. doi:. PMID 26410904.
- ↑ «AmtDB: a database of ancient human mitochondrial genomes». Nucleic Acids Research 47 (D1): D29–D32. January 2019. doi:. PMID 30247677.
- ↑ «InterMitoBase: an annotated database and analysis platform of protein-protein interactions for human mitochondria». BMC Genomics 12: 335. June 2011. doi:. PMID 21718467.
- ↑ «MitoBreak: the mitochondrial DNA breakpoints database». Nucleic Acids Research 42 (Database issue): D1261-8. January 2014. doi:. PMID 24170808.
- ↑ «MitoFish and MitoAnnotator: a mitochondrial genome database of fish with an accurate and automatic annotation pipeline». Molecular Biology and Evolution 30 (11): 2531–40. November 2013. doi:. PMID 23955518. PMC 3808866. https://archive.org/details/sim_molecular-biology-and-evolution_2013-11_30_11/page/2531.
- ↑ «Establishment of a mitochondrial DNA sequence database for the identification of fish species commercially available in South Africa». Molecular Ecology Resources 11 (6): 979–91. November 2011. doi:. PMID 21689383.
- ↑ «Mitome: dynamic and interactive database for comparative mitochondrial genomics in metazoan animals». Nucleic Acids Research 36 (Database issue): D938-42. January 2008. doi:. PMID 17940090.
- ↑ «MitoRes: a resource of nuclear-encoded mitochondrial genes and their products in Metazoa». BMC Bioinformatics 7: 36. January 2006. doi:. PMID 16433928.
- ↑ «MitoSatPlant: mitochondrial microsatellites database of viridiplantae». Mitochondrion 19 Pt B: 334–7. November 2014. doi:. PMID 24561221.
- ↑ «MitoZoa 2.0: a database resource and search tools for comparative and evolutionary analyses of mitochondrial genomes in Metazoa». Nucleic Acids Research 40 (Database issue): D1168-72. January 2012. doi:. PMID 22123747.
- ↑ «Mothers can influence offspring's height, lifespan and disease risk through mitochondria» (στα αγγλικά). phys.org. https://phys.org/news/2021-05-mothers-offspring-height-lifespan-disease.html. Ανακτήθηκε στις 14 June 2021.
- ↑ Yonova-Doing, Ekaterina; Calabrese, Claudia; Gomez-Duran, Aurora; Schon, Katherine; Wei, Wei; Karthikeyan, Savita; Chinnery, Patrick F.; Howson, Joanna M. M. (2021-05-17). «An atlas of mitochondrial DNA genotype–phenotype associations in the UK Biobank» (στα αγγλικά). Nature Genetics: 1–12. doi:. ISSN 1546-1718. PMID 34002094. https://www.nature.com/articles/s41588-021-00868-1. Ανακτήθηκε στις 14 June 2021.
Εξωτερικοί σύνδεσμοι Επεξεργασία
- Πολυμέσα σχετικά με το θέμα Mitochondrial DNA στο Wikimedia Commons