1-βρωμοβουτάνιο
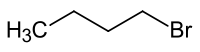
To 1-βρωμοβουτάνιο ή 1-βουτυλοβρωμίδιο είναι ένα υγρό (στις συνηθισμένες συνθήκες, T = 25 °C, P = 1 atm) αλκυλογονίδιο. Με βάση το χημικό τύπο του, C4H9F, έχει τα ακόλουθα τρία (3) ισομερές θέσης:
| 1-βρωμοβουτάνιο | |||
|---|---|---|---|
| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | 1-βρωμοβουτάνιο | ||
| Άλλες ονομασίες | 1-βουτυλοβρωμίδιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C4H9Br | ||
| Μοριακή μάζα | 92,57 amu | ||
| Σύντομος συντακτικός τύπος |
CH3CH2CH2CH2Br | ||
| Συντομογραφίες | BuBr | ||
| Αριθμός CAS | 109-65-9 | ||
| SMILES | CCCCBr | ||
| InChI | 1S/C4H9Br/c1-2-3-4-5/h2-4H2,1H3 | ||
| Αριθμός EINECS | 203-691-9 | ||
| Αριθμός RTECS | EJ6225000 | ||
| Αριθμός UN | 1126 | ||
| PubChem CID | 8002 | ||
| ChemSpider ID | 7711 | ||
| Δομή | |||
| Ισομέρεια | |||
| Ισομερή θέσης | 3 2-βρωμοβουτάνιο 1-βρωμομεθυλοπροπάνιο 2-βρωμομεθυλοπροπάνιο | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -112 °C | ||
| Σημείο βρασμού | 99-103 °C | ||
| Πυκνότητα | 1.267,6 kg/m3 | ||
| Δείκτης διάθλασης , nD |
1,439 | ||
| Τάση ατμών | 5,3 kPa | ||
| Εμφάνιση | Άχρωμο υγρό | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
10 °C | ||
| Σημείο αυτανάφλεξης | 265 °C | ||
| Επικινδυνότητα | |||
  
| |||
| Φράσεις κινδύνου | R11, R36/37/38, R51/53 | ||
| Φράσεις ασφαλείας | S16, S26 | ||
| LD50 | 2,761 g/kg | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Ονοματολογία Επεξεργασία
Η ονομασία «βρωμοβουτάνιο» προέρχεται από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το πρόθεμα «βουτ-» δηλώνει την παρουσία τεσσάρων (4) ατόμων άνθρακα ανά μόριο της ένωσης, το ενδιάμεσο «-αν-» δείχνει την παρουσία μόνο απλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες που έχουν χαρακτηριστικές καταλήξεις. Το αρχικό πρόθεμα «βρωμο-» δηλώνει την παρουσία ενός (1) ατόμου βρωμίου ανά μόριο της ένωσης. Τέλος, ο αρχικός αριθμός θέσης «1-», δηλώνει τον αριθμό θέσης του ατόμου του άνθρακα με το οποίο ενώνεται το άτομο του χλωρίου, για να διαχωριστεί η ένωση από την ισομερή της 2-βρωμοβουτάνιο.
Μοριακή δομή Επεξεργασία
| Δεσμοί[1] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C-H | σ | 2sp3-1s | 109 pm | 3% C- H+ |
| C-C | σ | 2sp3-2sp3 | 154 pm | |
| C-Br | σ | 2sp3-4sp3 | 191 pm | 2% C+ Br- |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| H | +0,03 | |||
| C#2,#3 | -0,06 | |||
| C#1 | -0,04 | |||
| Br | -0,02 | |||
| C#4 | -0,09 | |||
Παραγωγή Επεξεργασία
Με φωτοχημική βρωμίωση Επεξεργασία
Με φωτοχημική βρωμίωση βουτανίου παράγεται μίγμα 1-βρωμοβουτανίου και 2-βρωμοβουτανίου[2]:
- Ακολουθεί το συνηθισμένο μηχανισμό φωτοχημικής αλογόνωσης αλκανίων. Παράγονται και πολυβρωμοπαράγωγα. Η συγκέντρωση των τελευταίων περιορίζεται με χρήση περίσσειας βουτανίου.
- Η αναφερόμενη στοιχειομετρική αναλογία παραγωγής βρωμοβουτανίων δεν συνυπολογίζει τα συμπαραγόμενα πολυβρωμοπαράγωγα.
- Η μέθοδος δεν είναι χρήσιμη αν επιθυμείται το ένα μόνο ισομερές, αφού είναι σχετικά δύσκολος ο διαχωρισμός τους.
Υποκατάσταση υδροξυλίου από βρώμιο Επεξεργασία
1. Με επίδραση υδροβρωμίου (HCl) σε 1-βουτανόλη[3]:
2. Η υποκατάσταση του OH από Br στη 1-βουτανόλη μπορεί να γίνει και με βρωμιωτικά μέσα[4] Με τριβρωμιούχο φωσφόρο (PCl3)[5]:
Με προσθήκη βρωμαιθανίου σε αιθένιο Επεξεργασία
Με προσθήκη βρωμαιθάνιου σε αιθένιο παράγεται 1-βρωμοβουτάνιο[6]::
Με προσθήκη βρωμομεθανίου σε κυκλοπροπάνιο Επεξεργασία
Με προσθήκη βρωμομεθανίου σε κυκλοπροπάνιο παράγεται 1-βρωμοβουτάνιο[7]:
Με προσθήκη υδροβρωμίου σε κυκλοβουτάνιο Επεξεργασία
Με προσθήκη υδροβρωμίου (ΗBr) σε κυκλοβουτάνιο παράγεται 1-βρωμοβουτάνιο[8]:
Με αποικοδόμηση τύπου Hunsdiecker Επεξεργασία
Με επίδραση βρωμίου σε πεντανικό άργυρο παράγεται 1-βρωμοβουτάνιο - Αντίδραση Hunsdiecker[9]:
Χημικές ιδιότητες και παράγωγα Επεξεργασία
Αντιδράσεις υποκατάστασης Επεξεργασία
- Οι αντιδράσεις είναι πιο γρήγορες σε σύγκριση με τα αντίστοιχα αλκυλαλογονίδια των άλλων αλογόνων, πλην του ιωδίου.
Υποκατάσταση από υδροξύλιο Επεξεργασία
Κατά την υδρόλυσή του με εναιώρημα υδροξειδίου του αργύρου (AgOH) σχηματίζεται 1-βουτανόλη (CH3CH2CH2CH2OH)[10]:
Υποκατάσταση από αλκοξύλιο Επεξεργασία
Με αλκοολικά άλατα (RONa) σχηματίζει αλκυλoβουτυλαιθέρα (CH3CH2CH2CH2OR)[10]:
Υποκατάσταση από αλκινύλιο Επεξεργασία
Με αλκινικά άλατα (RC≡CNa) σχηματίζει αλκίνιο (RC≡CCH2CH2CH2CH3). Π.χ.[10]:
Υποκατάσταση από ακύλιο Επεξεργασία
Με καρβονικά άλατα (RCOONa) σχηματίζει καρβονικό βουτυλεστέρα (RCOOCH2CH2CH2CH3)[10]:
Υποκατάσταση από κυάνιο Επεξεργασία
Με κυανιούχο νάτριο (NaCN) σχηματίζει πεντανονιτρίλιο (CH3CH2CH2CH2CN)[10]:
Υποκατάσταση από αλκύλιο Επεξεργασία
Με αλκυλολίθιο (RLi) σχηματίζει αλκάνιο[10]:
Υποκατάσταση από σουλφυδρίλιο Επεξεργασία
Με όξινο θειούχο νάτριο (NaSH) σχηματίζει 1-βουτανοθειόλη (CH3CH2CH2CH2SH)[10]:
Υποκατάσταση από σουλφαλκύλιο Επεξεργασία
Με θειολικό νάτριο (RSNa) σχηματίζει αλκυλοβουτυλοθειαιθέρα (RSCH2CH2CH2CH3)[10]:
Υποκατάσταση από ιώδιο Επεξεργασία
Με ιωδιούχο νάτριο (NaI) σχηματίζει 1-ιωδοβουτάνιο (CH3CH2CH2CH2I)[10]:
Υποκατάσταση από φθόριο Επεξεργασία
Με επίδραση φθοριούχου υφυδραργύρου (Hg2F2) σε 1-βρωμοβουτάνιο (CH3CH2CH2CH2Br) παράγεται 1-φθοροβουτάνιο[11]:
Υποκατάσταση από αμινομάδα Επεξεργασία
Με αμμωνία (NH3) σχηματίζει 1-βουταναμίνη (CH3CH2CH2CH2NH2)[10]:
Υποκατάσταση από αλκυλαμινομάδα Επεξεργασία
Με πρωυτοταγείς αμίνες (RNH2) σχηματίζει N-αλκυλο-1-βουταναμίνη (RNHCH2CH2CH2CH3)[10]:
Υποκατάσταση από διαλκυλαμινομάδα Επεξεργασία
Με δευτεροταγείς αμίνες (R'NHR) σχηματίζει N,N-διαλκυλο-1-βουταναμίνη [R'N(CH2CH2CH2CH3)R][10]:
Υποκατάσταση από τριαλκυλαμινομάδα Επεξεργασία
Με τριτοταγείς αμίνες [R'N(R)R"] σχηματίζει βρωμιούχο N,N,N-τριαλκυλοβουτυλαμμώνιο {[R'N(CH2CH2CH2CH3)(R)R"]Br}[12]:
Υποκατάσταση από φωσφύλιο Επεξεργασία
Με φωσφίνη σχηματίζει 1-βουτανοφωσφαμίνη[13]:
Υποκατάσταση από νιτροομάδα Επεξεργασία
Με νιτρώδη άργυρο (AgNO2) σχηματίζει 1-νιτροβουτάνιο (CH3CH2CH2CH2NO2)[14]:
Υποκατάσταση από φαινύλιο Επεξεργασία
Με επίδραση τύπου Brriedel-Crafts σε βενζολίου παράγεται βουτυλοβενζόλιο:
Παραγωγή οργανομεταλλικών ενώσεων Επεξεργασία
1. Με λίθιο (Li σχηματίζει βουτυλολίθιο[15][16]:
2. Με μαγνήσιο (Mg) σχηματίζει βουτυλομαγνησιοβρωμίδιο [17]:
Αναγωγή Επεξεργασία
1. Με λιθιοαργιλλιοϋδρίδιο (LiAlH4) παράγεται βουτάνιο.[18]:
2. Με «υδρογόνο εν τω γενάσθαι», δηλαδή μέταλλο + οξύ παράγεται βουτάνιο.[19]:
3. Με σιλάνιο, παρουσία τριβρωμιούχου βορίου, παράγεται βουτάνιο[20]:
4. Αναγωγή από ένα αλκυλοκασσιτεράνιο. Π.χ.[21]:
Αντιδράσεις προσθήκης Επεξεργασία
1. Σε αλκένια. Π.χ. με αιθένιο (CH2=CH2) παράγει 1-βρωμεξάνιο (CH3CH2CH2CH2CH2CH2Br)[22]:
2. Σε αλκίνια. Π.χ. με αιθίνιο (HC≡CH) παράγει 1-βρωμο-1-εξένιο (CH3CH2CH2CH2CH=CHBr)[23]:
3. Η αντίδραση του 1-βρωμοβουτανίου με συζυγή αλκαδιένια αντιστοιχεί κυρίως σε 1,4-προσθήκη, αν και είναι επίσης δυνατές η 1,2-προσθήκη και η 3,4-προσθήκη, με τη χρήση κατάλληλων συνθηκών. Π.χ[24]:
(1,4-προσθήκη)
(1,2-προσθήκη)
(3,4-προσθήκη)
4. Σε κυκλοαλκάνια που έχουν τριμελή ή τετραμελή δακτύλιο. Π.χ. με κυκλοπροπάνιο παράγει 1-βρωμεπτάνιο[25]:
5. Σε ετεροκυκλικές ενώσεις που έχουν τριμελή ή τετραμελή δακτύλιο. Π.χ. με εποξυαιθάνιο παράγει βουτοξυ-2-βρωμαιθάνιο[26]:
Αντίδραση απόσπασης Επεξεργασία
Με απόσπαση υδροβρωμίου (HBr) από 1-βρωμοβουτάνιο παράγεται 1-βουτένιο[27]:
Παρεμβολή καρβενίων Επεξεργασία
- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε;
- 1. Παρεμβολή στους τρεις (3) δεσμούς CH2-H. Παράγεται 1-βρωμοπεντάνιο.
- 2. Παρεμβολή στους δυο (2) δεσμούς C#2H-H: Παράγεται 1-βρωμο-2-μεθυλοβουτάνιο.
- 3. Παρεμβολή στους δυο (2) δεσμούς C#3H-H: Παράγεται 1-βρωμο-3-μεθυλοβουτάνιο.
- 4. Παρεμβολή στους δυο (2) δεσμούς C#1H-H: Παράγεται 2-βρωμοπεντάνιο.
Προκύπτει επομένως μίγμα 1-βρωμοπεντάνιου ~33%, 1-βρωμο-2-μεθυλο-=βουτάνιου ~22%, 1-βρωμο-3-μεθυλοβουτάνιου ~22% και 2-βρωμοπεντάνιου ~22%.
Σημειώσεις και αναφορές Επεξεργασία
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 155, §6.7.2, R = CH3CH2CH2CH2, CH3CH2CHCH3, X = Br.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 185, §7.2.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 185, §7.2.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 185, §7.2.2, R = CH2CH2CH2CH3.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, για Ε = CH2CH3 και Nu = Br.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, εφαρμογή για κυκλοαλκάνια και για Ε = CH3 και Nu = Br σε συνδυασμό με Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §1.2., σελ. 22-25
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, εφαρμογή για κυκλοαλκάνια και για Ε = Η και Nu = Br σε συνδυασμό με Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §1.2., σελ. 22-25
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.3δ.
- ↑ 10,00 10,01 10,02 10,03 10,04 10,05 10,06 10,07 10,08 10,09 10,10 10,11 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 186, §7.3.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 185, §7.2.8.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 243, §10.2.Α, R = CH2CH2CH2CH3, X = Br.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 267, §11.3.Α1, R = CH3CH2CH2CH2, X = Br.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 244, §10.3.Α, R = CH2CH2CH2CH3, X = Br.
- ↑ Brandsma, L.; Verkraijsse, H. D. (1987). Preparative Polar Organometallic Chemistry I. Berlin: Springer-Verlag. ISBN 3-540-16916-4.
- ↑ Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991, §5.1. σελ.82
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 187, §7.3.5, R = CH2CH2CH2CH3, X = Br.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 187, §7.3.3α, R = CH2CH2CH2CH3, X = Br.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 187, §7.3.3β, R = CH2CH2CH2CH3, X = Br.
- ↑ Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991, σελ. 291-293, §19.1.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, Σελ. 42, §4.3.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, για Ε = CH3CH2CH2CH2 και Nu = Br.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, εφαρμογή για αλκίνια και για Ε = CH3CH2CH2CH2 και Nu = Br με βάση και την §8.1, σελ. 114-116.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, εφαρμογή για αλκαδιένια και για Ε = CH3CH2CH2CH2 και Nu = Br με βάση και την §8.2, σελ. 116-117.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, εφαρμογή για κυκλοαλκάνια και για Ε = CH3CH2CH2CH2 και Nu = Br σε συνδυασμό με Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §1.2., σελ. 22-25
- ↑ Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §2.1., σελ. 16-17, εφαρμογή γενικής αντίδρασης για Nu = Br.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.1α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 155, §6.7.3.
Πηγές Επεξεργασία
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985