Υπερκρίσιμο διοξείδιο του άνθρακα
Ο χημικός όρος υπερκρίσιμο διοξείδιο του άνθρακα (σύμβολο: sCO2) αναφέρεται στη φάση υπερκρίσιμου ρευστού του διοξειδίου του άνθρακα (CO2), όπου αυτό διατηρείται ή βρίσκεται υπεράνω από την κρίσιμη θερμοκρασία του και την κρίσιμη πίεσή του.
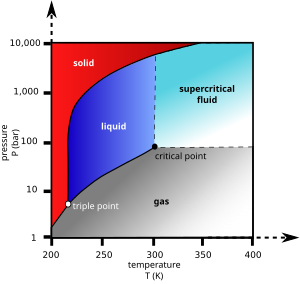
Το διοξείδιο του άνθρακα τυπικά συμπεριφέρεται ως αέριο στον αέρα υπό κανονικές συνθήκες θερμοκρασίας και πίεσης (ΚΣ), ή ως στερεό που ονομάζεται ξηρός πάγος όταν ψύχεται ή/και συμπιέζεται επαρκώς. Εάν η θερμοκρασία και η πίεση αυξηθούν και οι δύο πέραν από τις ΚΣ για να προσεγγίσουν στο κρίσιμο σημείο ή πάνω από το κρίσιμο σημείο για το διοξείδιο του άνθρακα, μπορεί τότε το CO2 να εμφανίσει ιδιότητες σχεδόν μεταξύ ενός αερίου και ενός υγρού. Πιο συγκεκριμένα, το CO2 συμπεριφέρεται ως υπερκρίσιμο ρευστό πάνω από την κρίσιμη θερμοκρασία του (ήτοι: >30,9780°C)[1] και την κρίσιμη πίεσή του (ήτοι: >72,808 atm),[1] διαστέλλεται ούτως ώστε να πληρώσει ένα δοχείο σαν ένα αέριο αλλά με πυκνότητα όπως αυτή του υγρού.
Το υπερκρίσιμο CO2 αποτελεί πλέον σημαντικό εμπορικό και βιομηχανικό διαλύτη λόγω του καθοριστικού ρόλου του στη χημική εκχύλιση, αφού πλεονεκτεί και για τη σχετικά χαμηλή τοξικότητά του αλλά και για τις ελάχιστες περιβαλλοντικές επιπτώσεις του. Η σχετικά χαμηλή θερμοκρασία της διεργασίας και η σταθερότητα του CO2 επιτρέπει σαφώς αποτελεσματικότερη εκχύλιση των περισσότερων ενώσεων με μικρή ζημία, ή με χαμηλότατο έως μηδενικό κίνδυνο μετουσίωσης των. Επιπλέον, η αυξημένη διαλυτότητα πολλών ενώσεων - δηλ. εκχυλισμάτων - σε CO2 μεταβάλλεται ανάλογα με την πίεση,[2] επιτρέποντας έτσι και επιλεκτικές εκχυλίσεις.
Τελικές εφαρμογές Επεξεργασία
Ως διαλύτης Επεξεργασία
Το διοξείδιο του άνθρακα κερδίζει σε δημοτικότητα μεταξύ των παρασκευαστών καφέ, που επιθυμούν να απομακρυνθούν από τους τυπικούς διαλύτες ντεκαφεϊνέ. Το sCO2 διοχετεύεται μέσω των πράσινων κόκκων καφέ που στη συνέχεια ψεκάζονται με νερό σε υψηλή πίεση για να αφαιρεθεί η καφεΐνη. Στη συνέχεια, η καφεΐνη μπορεί να απομονωθεί για μεταπώληση (π.χ. στους παρασκευαστές φαρμάκων ή/και ποτών) με χρήση ύδατος μέσω φίλτρων ενεργού άνθρακα ή με απόσταξη, ή κρυστάλλωση ή με αντίστροφη ώσμωση.
Πρόσθετα, το υπερκρίσιμο διοξείδιο του άνθρακα χρησιμοποιείται για την έκπλυση οργανοχλωριδικών φυτοφαρμάκων και μετάλλων από γεωργικές καλλιέργειες, χωρίς να νοθεύονται τα δραστικά συστατικά από τη φυτική ύλη στη βιομηχανία των φυτικών συμπληρωμάτων.[3]
Το υπερκρίσιμο διοξείδιο του άνθρακα μπορεί να χρησιμοποιηθεί ως πιο φιλικός προς το περιβάλλον διαλύτης για το στεγνό καθάρισμα έναντι παραδοσιακών διαλυτών όπως π.χ. οι χλωράνθρακες, συμπεριλαμβανομένου του υπερχλωροαιθυλενίου.[4]
Το υπερκρίσιμο διοξείδιο του άνθρακα χρησιμοποιείται ως διαλύτης εκχύλισης για τη ανάκτηση αιθέριων ελαίων και άλλων φυτικών αποσταγμάτων[5] από φυσικά προϊόντα. Τα κύρια πλεονεκτήματά του έναντι των διαλυτών, λ.χ. έναντι του εξανίου και της ακετόνης, σε αυτή τη διαδικασία είναι ότι δεν είναι εύφλεκτο και δεν αφήνει τοξικά υπολείμματα ή παραπροϊόντα. Επιπλέον, ο διαχωρισμός των συστατικών της αντίδρασης από το αρχικό υλικό είναι πολύ απλούστερος από ότι με τους συμβατικούς κοινούς, πολικούς ή μη πολικούς οργανικούς διαλύτες. Το CO2 μπορεί να εξατμιστεί στον αέρα ή/και να ανακυκλωθεί με συμπύκνωση σε δοχείο ανάκτησης ψυχρού. Το πλεονέκτημά του έναντι της απόσταξης με ατμό είναι ότι δρα σε εξόχως χαμηλή θερμοκρασία (πλεονέκτημα σημαντικότατο), η οποία μπορεί να διαχωρίσει τους φυσικούς κηρούς από τα έλαια.[6]
Στα εργαστήρια, το sCO2 χρησιμοποιείται ως διαλύτης για εκχύλιση, για παράδειγμα, για τον προσδιορισμό των συνολικών ανακτήσιμων υδρογονανθράκων από εδάφη, ιζήματα, ιπτάμενη τέφρα [7] και για προσδιορισμό πολυκυκλικών αρωματικών υδρογονανθράκων (ΠΑΥ) στο έδαφος και τα στερεά απόβλητα.[8] Η εξαγωγή υπερκρίσιμου ρευστού έχει χρησιμοποιηθεί και για τον προσδιορισμό των συστατικών υδρογονανθράκων στο νερό.[9]
Διεργασίες που χρησιμοποιούν sCO2 για την παραγωγή σωματιδίων μικρο- και νανο- κλίμακας, συχνά για φαρμακευτικές χρήσεις, βρίσκονται σήμερα ήδη υπό ανάπτυξη. Η διαδικασία αέριων αντιδιαλυτών, η ταχεία διαστολή υπερκρίσιμων διαλυμάτων και η κατακρήμνιση υπερκρίσιμου αντιδιαλύτη (καθώς και αρκετές συναφείς μέθοδοι) επεξεργάζονται ποικιλία ουσιών σε σωματίδια.[10]
Λόγω της εξαιρετικής ιδιότητάς του να διαλύει επιλεκτικά οργανικές ενώσεις και να επιβοηθά στη λειτουργία των ενζύμων, το υπερκρίσιμο CO2 έχει προταθεί ως πιθανός διαλύτης για την υποστήριξη της βιολογικής δραστηριότητας που ενδεχομένως υπάρχει σε πλανήτες, όπως λ.χ. Αφροδίτη ή σε εξωηλιακούς πλανήτες.[11]
Για πολυμερικά προϊόντα Επεξεργασία
Τα φιλικά προς το περιβάλλον, υποκατάστατα χαμηλού κόστους για άκαμπτο θερμοπλαστικό και ψημένα κεραμικά συντίθενται με χρήση sCO2 ως χημικό αντιδραστήριο. Το sCO2 σε αυτές τις διεργασίες αντιδρά με τα αλκαλικά συστατικά του πλήρως σκληρυμένου υδραυλικού τσιμέντου ή του γύψου για να σχηματιστούν διάφορα ανθρακικά.[12] Το κύριο παραπροϊόν είναι το νερό.
Το υπερκρίσιμο διοξείδιο του άνθρακα χρησιμοποιείται στον αφρισμό πολυμερών. Το υπερκρίσιμο διοξείδιο του άνθρακα μπορεί να προκαλέσει κατάλυση στο πολυμερές με τον διαλύτη. Κατά την αποσυμπίεση και τη θέρμανση, το διοξείδιο του άνθρακα διαστέλλεται γρήγορα, προκαλώντας κενά μέσα στη μήτρα του πολυμερούς, δηλαδή δημιουργώντας αφρό. Έρευνες υπό εξέλιξη σε πολλά πανεπιστήμια εκπονούνται σήμερα για την παραγωγή μικροκυτταρικού αφρού με χρήση του sCO2.
Μια ειδική διεργασία για ηλεκτροχημική καρβοξυλίωση ενός παρα-ισοβουτυλοβενζυλοχλωριδίου σε ιβουπροφαίνη προωθείται σήμερα με την βοήθεια του sCO2.[13]
Σε ρευστά Επεξεργασία
Το υπερκρίσιμο CO2 είναι χημικά σταθερό, αξιόπιστο, σχετικά χαμηλού κόστους, μη εύφλεκτο και άμεσα διαθέσιμο, καθιστώντας το έτσι επιθυμητό ρευστό για διακρίσιμους κύκλους.[14]
Το υπερκρίσιμο διοξείδιο χρησιμοποιείται επίσης ως ρευστό σε οικιακές αντλίες θερμότητας νερού με υψηλή απόδοση. Οι αντλίες θερμότητας που κατασκευάζονται και χρησιμοποιούνται ευρέως διατίθενται επίσης στο εμπόριο για οικιακή και επαγγελματική θέρμανση και ψύξη.[14] Ενώ μερικές από τις πιο κοινές αντλίες θερμότητας νερού οικιακής χρήσης αφαιρούν τη θερμότητα από το χώρο στον οποίο βρίσκονται, όπως ένα υπόγειο ή γκαράζ, οι θερμοσίφωνες με αντλία θερμότητας τεχνολογίας CO2 βρίσκονται συνήθως έξω, όπου απομακρύνουν τη θερμότητα από τον εξωτερικό αέρα.[14]
Παραγωγή ηλεκτρικής ενέργειας Επεξεργασία
Οι μοναδικές ιδιότητες του sCO2 παρουσιάζουν πλεονεκτήματα για την παραγωγή ηλεκτρικής ενέργειας κλειστού βρόχου και μπορούν να εφαρμοστούν σε διάφορες εφαρμογές παραγωγής ενέργειας. Τα συστήματα παραγωγής ενέργειας που χρησιμοποιούν συμβατικούς κύκλους Rankine με αέρα Brayton και ατμού μπορούν να αναβαθμιστούν σε τεχνολογίας sCO2 για αύξηση της απόδοσης και της ισχύος εξόδου.
Ο σχετικά νέος κύκλος ισχύος Allam χρησιμοποιεί το sCO2 ως υγρό εργασίας σε συνδυασμό με καύσιμο και καθαρό οξυγόνο. Το CO2 που παράγεται από την καύση αναμιγνύεται με το ρευστό εργασίας sCO2 και μια αντίστοιχη ποσότητα καθαρού CO2 πρέπει να αφαιρεθεί από τη διαδικασία (για βιομηχανική χρήση ή για δέσμευση). Αυτή η διαδικασία μειώνει τις ατμοσφαιρικές εκπομπές σχεδόν στο μηδέν.
Παρουσιάζει ενδιαφέρουσες ιδιότητες που υπόσχονται ουσιαστικές βελτιώσεις στην απόδοση του εν γένει συστήματος. Λόγω της υψηλής πυκνότητάς του, το sCO2 επιτρέπει την εξαιρετικά συμπαγή και εξόχως αποδοτική στροβιλομηχανή. Μπορεί να χρησιμοποιεί απλούστερα ως σχέδια αμαξώματος με ένα περίβλημα, ενώ οι ατμοστρόβιλοι απαιτούν πολλαπλά στάδια στροβίλου και τα σχετικά περιβλήματα, καθώς και πρόσθετες σωληνώσεις εισόδου και εξόδου. Η υψηλή πυκνότητα επιτρέπει την εξαιρετικά συμπαγή τεχνολογία εναλλάκτη θερμότητας που βασίζεται σε μικροκάναλο.[15]
Το 2016, η αμερικανική εταιρεία General Electric παρουσίασε έναν υπερκρίσιμο στρόβιλο με βάση το sCO2 που επέτρεψε την απόδοση 50% της μετατροπής της θερμικής ενέργειας σε ηλεκτρική ενέργεια. Σε αυτήν την τεχνική, το CO2 θερμαίνεται στους 700 °C. Απαιτεί λιγότερη συμπίεση και επιτρέπει τη μεταφορά θερμότητας. Φτάνει δε, σε πλήρη ισχύ σε 2 λεπτά, ενώ οι ατμοστρόβιλοι χρειάζονται τουλάχιστον 30 λεπτά. Το πρωτότυπο μοντέλο στροβίλου φτάνει τα 10 MW και είναι περίπου 10% του μεγέθους ενός αντίστοιχου, συμβατικού σήμερα ατμοστρόβιλου.[16]
Για συγκεντρωμένη ηλιακή ενέργεια, η κρίσιμη θερμοκρασία του διοξειδίου του άνθρακα δεν είναι αρκετά υψηλή για να επιτευχθεί η μέγιστη απόδοση μετατροπής ενέργειας. Οι ηλιακές θερμικές εγκαταστάσεις βρίσκονται συνήθως σε ξηρές περιοχές, επομένως, είναι αδύνατο να ψυχθεί η ψύκτρα σε υποκρίσιμες θερμοκρασίες. Ως εκ τούτου, τα υπερκρίσιμα μείγματα διοξειδίου του άνθρακα, με υψηλότερες κρίσιμες θερμοκρασίες, αναπτύσσονται για τη βελτίωση της παραγωγής της ηλεκτρικής ενέργειας με τεχνολογία συγκεντρωμένης ηλιακής ακτινοβολίας.
Περαιτέρω, λόγω της ανώτερης θερμικής σταθερότητας και της μη ευφλεκτότητάς του, είναι δυνατή η άμεση ανταλλαγή θερμότητας από πηγές υψηλής θερμοκρασίας, επιτρέποντας υψηλότερες θερμοκρασίες ρευστού εργασίας και επομένως υψηλότερη απόδοση κύκλου. Σε αντίθεση με τη διφασική ροή, η μονοφασική φύση του sCO2 εξαλείφει την ανάγκη εισόδου θερμότητας για αλλαγή φάσης που απαιτείται για τη μετατροπή νερού σε ατμό, εξαλείφοντας έτσι και τη σχετική θερμική κόπωση αλλά και τη διάβρωση.[17]
Παρά τις προσδοκίες για σημαντικά υψηλότερη απόδοση και χαμηλότερο κόστος κεφαλαίου, η χρήση του sCO2 παρουσιάζει θέματα μηχανικής διάβρωσης, επιλογής υλικού και σχεδιασμού. Τα υλικά στα εξαρτήματα παραγωγής ενέργειας πρέπει να παρουσιάζουν αντοχή σε ζημιές που προκαλούνται από υψηλή θερμοκρασία, οξείδωση και (μηχανικό) ερπυσμό. Πιθανά υλικά που πληρούν αυτούς τους στόχους κατάλληλων ιδιοτήτων και απόδοσης περιλαμβάνουν υφιστάμενα κράματα στην παραγωγή ενέργειας, όπως υπερκράματα με βάση το νικέλιο για εξαρτήματα στροβιλομηχανών και ωστενιτικούς ανοξείδωτους χάλυβες για σωληνώσεις. Εξαρτήματα εντός του sCO2 π.χ. βρόχοι Brayton, έχουν ευαισθησία σε διάβρωση, συγκεκριμένα π.χ. διάβρωση σε στροβιλομηχανές και εξαρτήματα εναλλάκτη θερμότητας ανάκτησης και διακοκκώδη διάβρωση ή/και διάβρωση στις σωληνώσεις.[18]
Έχουν διεξαχθεί δοκιμές σε πιθανώς κατάλληλα κράματα με βάση το Ni, ωστενιτικούς χάλυβες, φερριτικούς χάλυβες και κεραμικά, για αντοχή στη διάβρωση, σε πολλαπλούς κύκλους με sCO2. Το ενδιαφέρον για αυτά τα υλικά προέρχεται από το σχηματισμό προστατευτικών επιφανειακών στρωμάτων οξειδίου παρουσία διοξειδίου του άνθρακα, ωστόσο, στις περισσότερες περιπτώσεις απαιτείται περαιτέρω αξιολόγηση της μηχανικής αντίδρασης και της κινητικής και των μηχανισμών διάβρωσης, καθώς κανένα από τα υλικά δεν πληροί τους απαραίτητους στόχους.[19][20]
Διάφορα Επεξεργασία
Σήμερα διενεργούνται δοκιμές για την ανάπτυξη ενός συστήματος - με βάση το sCO2 - αεριοστρόβιλου κλειστού κύκλου για λειτουργία σε θερμοκρασίες κοντά στους 550°C. Αυτό θα είχε συνέπειες για τη μαζική θερμική και πυρηνική παραγωγή ηλεκτρικής ενέργειας, επειδή οι υπερκρίσιμες ιδιότητες του διοξειδίου του άνθρακα πάνω από 500 °C και σε πιέσεις >200 Atm επιτρέπουν τη θερμική απόδοση που πλησιάζει το 45 τοις εκατό. Αυτό θα μπορούσε να αυξήσει την ηλεκτρική ισχύ που παράγεται ανά μονάδα καυσίμου που απαιτείται κατά 40 τοις εκατό ή περισσότερο. Δεδομένου του όγκου των καυσίμων άνθρακα που χρησιμοποιούνται για την παραγωγή ηλεκτρικής ενέργειας, οι περιβαλλοντικές επιπτώσεις των αυξήσεων της απόδοσης του κύκλου θα είναι πολύ σημαντικές.[21]
Το υπερκρίσιμο CO2 είναι αναδυόμενο φυσικό ψυκτικό μέσο, που χρησιμοποιείται σε νέες λύσεις χαμηλών εκπομπών άνθρακα για οικιακές αντλίες θερμότητας. Αντλίες θερμότητας τεχνολογίας υπερκρίσιμου CO2 διατίθενται στο εμπόριο στην Ασία. Τα λεγόμενα συστήματα <b><i>EcoCute</i></b> από την Ιαπωνία, που αναπτύχθηκαν από την εταιρεία Mayekawa, αναπτύσσουν οικιακό νερό υψηλής θερμοκρασίας με μικρές εισροές ηλεκτρικής ενέργειας μεταφέροντας θερμότητα στο σύστημα από το περιβάλλον.[22]
Το υπερκρίσιμο CO2 έχει χρησιμοποιηθεί από τη δεκαετία του 1980 για την ενίσχυση της ανάκτησης σε ώριμα κοιτάσματα πετρελαίου.
Αναδύονται τεχνολογίες «καθαρού άνθρακα» που θα μπορούσαν να συνδυάσουν τέτοιες βελτιωμένες μεθόδους ανάκτησης με δέσμευση άνθρακα. Χρησιμοποιώντας αεριοποιητές αντί για συμβατικούς κλιβάνους, ο άνθρακας και το νερό ανάγονται σε: αέριο υδρογόνο, διοξείδιο του άνθρακα και τέφρα. Αυτό το αέριο υδρογόνο μπορεί να χρησιμοποιηθεί για την παραγωγή ηλεκτρικής ενέργειας σε αεριοστρόβιλους συνδυασμένου κύκλου, το δε, CO2 να συλλαμβάνεται, να συμπιέζεται στην υπερκρίσιμη φάση και να εγχέεται στη γεωλογική αποθήκευση, πιθανώς σε υπάρχοντα κοιτάσματα πετρελαίου για τη βελτίωση των αποδόσεων.[23][24][25]
Το υπερκρίσιμο CO2 μπορεί να χρησιμοποιηθεί ως λειτουργικό ρευστό για την παραγωγή γεωθερμικής ηλεκτρικής ενέργειας τόσο σε ενισχυμένα γεωθερμικά συστήματα[26][27] όσο και σε ιζηματογενή γεωθερμικά συστήματα (τα λεγόμενα CO2 Plume Geothermal).[28][29]
Τα συστήματα EGS χρησιμοποιούν μια δεξαμενή τεχνητής θραύσης σε βράχο του υπογείου, ενώ τα συστήματα CPG χρησιμοποιούν πιο ρηχές φυσικά διαπερατές ιζηματογενείς δεξαμενές. Πιθανά πλεονεκτήματα από τη χρήση CO2 σε μια γεωλογική δεξαμενή, σε σύγκριση με το νερό, περιλαμβάνουν υψηλότερη ενεργειακή απόδοση που προκύπτει από το χαμηλότερο ιξώδες, την καλύτερη χημική αλληλεπίδραση και το μόνιμο CO2 αποθήκευση καθώς η δεξαμενή πρέπει να γεμίσει με μεγάλες μάζες από CO2. Από το 2011, η ιδέα αυτή δεν είχε δοκιμαστεί στο πεδίο.[30]
Για παραγωγή αερογέλης Επεξεργασία
Το υπερκρίσιμο διοξείδιο του άνθρακα χρησιμοποιείται στην παραγωγή αεροπηκτωμάτων πυριτίου, άνθρακα και μετάλλων.
Για παράδειγμα, σχηματίζεται γέλη διοξειδίου του πυριτίου και στη συνέχεια εκτίθεται σε sCO2. Όταν το CO2 γίνεται υπερκρίσιμο, αφαιρείται όλη η επιφανειακή τάση, επιτρέποντας στο ρευστό να διαφύγει από το αεροπήκτωμα και να δημιουργήσει πόρους μεγέθους νανομέτρων.[31]
Για αποστείρωση βιοϊατρικών υλικών Επεξεργασία
Το υπερκρίσιμο CO2 είναι μια εναλλακτική λύση για τη θερμική αποστείρωση βιολογικών υλικών και ιατροτεχνολογικών προϊόντων με συνδυασμό του πρόσθετου υπεροξικού οξέος (PAA).
Το υπερκρίσιμο CO2 δεν αποστειρώνει τα μέσα, γιατί δεν θανατώνει τα σπόρια των μικροοργανισμών. Επιπλέον, αυτή η διαδικασία είναι ήπια, καθώς διατηρείται η μορφολογία, η υπερδομή και τα πρωτεϊνικά προφίλ των αδρανοποιημένων μικροβίων.[32]
Σε καθαρισμούς Επεξεργασία
Το υπερκρίσιμο CO2 χρησιμοποιείται και σε ορισμένες βιομηχανικές διαδικασίες καθαρισμού.
Δείτε επίσης Επεξεργασία
- Καφεΐνη
- Στεγνό καθάρισμα
- Άρωμα
- Υπερκρίσιμο ρευστό
- Στην ατμόσφαιρα της Αφροδίτης, σχεδόν όλο το διοξείδιο του άνθρακα είναι σε υπερκρίσιμη φάση
Παραπομπές Επεξεργασία
- ↑ 1,0 1,1 Span, Roland; Wagner, Wolfgang (1996). «A New Equation of State for Carbon Dioxide Covering the Fluid Region from the Triple‐Point Temperature to 1100 K at Pressures up to 800 MPa». Journal of Physical and Chemical Reference Data 25 (6): 1509–1596. doi:. Bibcode: 1996JPCRD..25.1509S.
- ↑ Discovery - Can Chemistry Save The World? - BBC World Service
- ↑ Department of Pharmaceutical Analysis, Shenyang Pharmaceutical University, Shenyang 110016, China
- ↑ Stewart, Gina (2003), Joseph M. DeSimone; William Tumas, επιμ., «Dry Cleaning with Liquid Carbon Dioxide», Green Chemistry Using Liquid and SCO2: 215–227
- ↑ Aizpurua-Olaizola, Oier; Ormazabal, Markel; Vallejo, Asier; Olivares, Maitane; Navarro, Patricia; Etxebarria, Nestor; Usobiaga, Aresatz (2015-01-01). «Optimization of supercritical fluid consecutive extractions of fatty acids and polyphenols from Vitis vinifera grape wastes». Journal of Food Science 80 (1): E101–107. doi:. ISSN 1750-3841. PMID 25471637.
- ↑ Mendiola, J.A.; Herrero, M.; Cifuentes, A.; Ibañez, E. (2007). «Use of compressed fluids for sample preparation: Food applications». Journal of Chromatography A 1152 (1–2): 234–246. doi:. PMID 17353022.
- ↑ «Test Methods | Wastes - Hazardous Waste | US EPA». wayback.archive-it.org. Αρχειοθετήθηκε από το πρωτότυπο στις 17 Δεκεμβρίου 2008. Ανακτήθηκε στις 17 Απριλίου 2023.
- ↑ U.S.EPA Method 3561 Supercritical Fluid Extraction of Polycyclic Aromatic Hydrocarbons.
- ↑ Use of Ozone Depleting Substances in Laboratories. TemaNord 2003:516.
- ↑ Yeo, S.; Kiran, E. (2005). «Formation of polymer particles with supercritical fluids: A review». J. Supercrit. Fluids 34 (3): 287–308. doi:.
- ↑ Budisa, Nediljko; Schulze-Makuch, Dirk (8 August 2014). «Supercritical Carbon Dioxide and Its Potential as a Life-Sustaining Solvent in a Planetary Environment». Life 4 (3): 331–340. doi:. PMID 25370376. Bibcode: 2014Life....4..331B.
- ↑ Rubin, James B.; Taylor, Craig M. V.; Hartmann, Thomas; Paviet-Hartmann, Patricia (2003), Joseph M. DeSimone; William Tumas, επιμ., «Enhancing the Properties of Portland Cements Using Supercritical Carbon Dioxide», Green Chemistry Using Liquid and Supercritical Carbon Dioxide: 241–255
- ↑ Sakakura, Toshiyasu; Choi, Jun-Chul; Yasuda, Hiroyuki (13 June 2007). «Transformation of Carbon dioxide». Chemical Reviews 107 (6): 2365–2387. doi:. PMID 17564481.
- ↑ 14,0 14,1 14,2 Ma, Yitai; Liu, Zhongyan; Tian, Hua (2013). «A review of transcritical carbon dioxide heat pump and refrigeration cycles». Energy 55: 156–172. doi:. ISSN 0360-5442. https://www.researchgate.net/publication/257177350.
- ↑ «Supercritical CO2 Power Cycle Developments and Commercialization: Why sCO2 can Displace Steam» (PDF).
- ↑ Talbot, David (11 Απριλίου 2016). «Desk-Size Turbine Could Power a Town». MIT Technology Review. Ανακτήθηκε στις 13 Απριλίου 2016.
- ↑ «Supercritical Carbon Dioxide Power Cycles Starting to Hit the Market». Breaking Energy.
- ↑ «Corrosion and Erosion Behavior in sCO2 Power Cycles» (PDF). Sandia National Laboratories.
- ↑ «THE EFFECT OF TEMPERATURE ON THE sCO2 COMPATIBILITY OF CONVENTIONAL STRUCTURAL ALLOYS» (PDF). The 4th International Symposium - Supercritical CO2 Power Cycles. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 23 Απριλίου 2016.
- ↑ J. Parks, Curtis. «Corrosion of Candidate High Temperature Alloys in Supercritical Carbon Dioxide» (PDF). Ottawa-Carleton Institute for Mechanical and Aerospace Engineering.
- ↑ V. Dostal, M.J. Driscoll, P. Hejzlar, «A Supercritical Carbon Dioxide Cycle for Next Generation Nuclear Reactors» (PDF). Ανακτήθηκε στις 20 Νοεμβρίου 2007. MIT-ANP-Series, MIT-ANP-TR-100 (2004)
- ↑ «Heat Pumps». Mayekawa Manufacturing Company (Mycom). Ανακτήθηκε στις 7 Φεβρουαρίου 2015.
- ↑ "The Hydrogen Economy: Opportunities, Costs, Barriers, and R&D Needs", p. 84 (2004)
- ↑ «FutureGen 2.0 Project». FutureGen Alliance. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Φεβρουαρίου 2015. Ανακτήθηκε στις 7 Φεβρουαρίου 2015.
- ↑ «Øyvind Vessia: "Fischer- Tropsch reactor fed by syngas"». Αρχειοθετήθηκε από το πρωτότυπο στις 29 Σεπτεμβρίου 2007.
- ↑ K Pruess(2007)Enhanced Geothermal Systems (EGS) comparing water with CO2 as heat transmission fluids"
- ↑ J Apps(2011), "Modeling geochemical processes in enhanced geothermal systems with CO2 as heat transfert fluid"
- ↑ Randolph, Jimmy B.; Saar, Martin O. (2011). «Combining geothermal energy capture with geologic carbon dioxide sequestration». Geophysical Research Letters 38 (L10401): n/a. doi:. Bibcode: 2011GeoRL..3810401R.
- ↑ Adams, Benjamin M.; Kuehn, Thomas H.; Bielicki, Jeffrey M.; Randolph, Jimmy B.; Saar, Martin O. (2015). «A comparison of electric power output of CO2 Plume Geothermal (CPG) and brine geothermal systems for varying reservoir conditions». Applied Energy 140: 365–377. doi:.
- ↑ http://earthsciences.typepad.com/blog/2011/06/achieving-carbon-sequestration-and-geothermal-energy-production-a-win-win.html ESD News and Events "Achieving Carbon Sequestration and Geothermal Energy Production: A Win-Win!"
- ↑ «Aerogel.org » Supercritical Drying».
- ↑ White, Angela; Burns, David; Christensen, Tim W. (2006). «Effective terminal sterilization using supercritical carbon dioxide». Journal of Biotechnology 123 (4): 504–515. doi:. PMID 16497403.
Περαιτέρω ανάγνωση Επεξεργασία
- Mukhopadhyay M. (2000). Natural extracts using supercritical carbon dioxide. United States: CRC Press, LLC. Free preview at Google Books.