1,2-αιθενοδιόλη
Η 1,2-αιθενοδιόλη ή 1,2-διυδροξυαιθένιο ή 1,2-διυδροξυαιθυλένιο (σε δύο (2) γεωμετρικά ισομερή) είναι μια ασταθής, αλκενοδιόλη, δηλαδή άκυκλη αλκοόλη με ένα διπλό δεσμό και δύο υδροξύλια. Συνήθως αντιπροσωπεύεται από τον τύπο CH2=C(OH)2. Με βάση το χημικό της τύπο, C2H4O2, είναι «τυπικός» υδατάνθρακας (δηλαδή έχει την αναλογία ατόμων υδρογόνου - οξυγόνου 2:1, που έχει και το νερό, αλλά χωρίς να είναι πραγματικό σάκχαρο) έχει τα ακόλουθα εννέα (9) ισομερή θέσης:
- Βινυλυδροϋπεροξείδιο ή βινυλοδιοξειδάνιο, υπεροξείδια με ημισυντακτικό τύπο CH2=CHO2H.
- 1,1-αιθενοδιόλη με ημισυντακτικό τύπο CH2=C(OH)2.
- Υδροξυαιθανάλη με ημισυντακτικό τύπο HOCH2CHO.
- Αιθανικό οξύ με ημισυντακτικό τύπο CH3COOH.
- Μεθανικός μεθυλεστέρας με ημισυντακτικό τύπο HCOOCH3.
- 1,2-διοξετάνιο ή 1,2-επιδιοξυαιθάνιο με γραμμικό τύπο
 .
. - 1,3-διοξετάνιο ή 1,1΄-εποξυμεθοξυμεθάνιο με γραμμικό τύπο
 .
. - Μεθυλοδιοξιράνιο ή 1,1-επιδιοξυαιθάνιο με γραμμικό τύπο
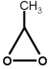 .
. - Οξιρανόλη ή 1,2-εποξυαιθανόλη με γραμμικό τύπο
 .
.
| 1,2-αιθενοδιόλη | |
|---|---|

| |

| |
| Γενικά | |
| Όνομα IUPAC | 1,2-αιθενοδιόλη |
| Άλλες ονομασίες | 1,2-διυδροξυαιθένιο 1,2-διυδροξυαιθυλένιο |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C2H4O2 |
| Μοριακή μάζα | 60,05 amu |
| Σύντομος συντακτικός τύπος |
HOCH=CHOH |
| SMILES | OC=CO |
| Δομή | |
| Μοριακή γεωμετρία | επίπεδη |
| Ισομέρεια | |
| Ισομερή θέσης | 9 |
| Γεωμετρικά ισομερή | 2 |
| Φυσικές ιδιότητες | |
| Χημικές ιδιότητες | |
| Αυτοϊσομερίωση | ναι προς υδροξυαιθανάλη |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
Δομή Επεξεργασία
Χημικές ιδιότητες και παράγωγα Επεξεργασία
Ταυτομέρεια Επεξεργασία
Βασική ιδιότητά της είναι η ταυτομέρεια με την υδροξυαιθανάλη, με την οποία βρίσκεται σε χημική ισορροπία, έντονα μετατοπισμένη σε όφελος της υδροξυαλδεΰδης[3]:
Αλογόνωση Επεξεργασία
Με επίδραση αλογόνου (X2) έχουμε προσθήκη στην αιθενοδιόλη-1,1, οπότε παράγεται αρχικά η ασταθής 1,2-διαλοαιθανοδιόλη-1,2, που αφυδραλογονώνεται σχηματίζοντας τελικά αιθανοδιάλη[4]:
Αναφορές και σημειώσεις Επεξεργασία
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ Υπολογισμένο βάση του ιονισμού από τον παραπάνω πίνακα
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.218, §9.5.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.220, §9.5.13.
Πηγές Επεξεργασία
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.



