Κερατίνη
H κερατίνη είναι ινώδης δομική πρωτεΐνη η οποία ανήκει στην οικογένεια των σκληροπρωτεϊνών. Η α-κερατίνη είναι ένας τύπος κερατίνης που βρίσκεται στα σπονδυλωτά. Είναι το βασικό δομικό υλικό από το οποίο αποτελούνται οι τρίχες, τα νύχια, τα φτερά, τα κέρατα, οι οπλές και το εξωτερικό στρώμα του δέρματος των σπονδυλωτών. Η κερατίνη προστατεύει επίσης τα επιθηλιακά κύτταρα από βλάβες ή καταπόνηση. Τα μονομερή κερατίνης συναρμολογούνται σε δεσμίδες για να σχηματίσουν τα ενδιάμεσα ινίδια, τα οποία είναι σκληρά και σχηματίζουν ισχυρές μη ασβεστοποιημένες επιδερμικές επιφάνειες που απαντώνται σε ερπετά, πτηνά, αμφίβια και θηλαστικά.[1][2]
Η κερατίνη είναι εξαιρετικά αδιάλυτη στο νερό και στους οργανικούς διαλύτες και ανθίσταται στην πέψη. Το μόνο άλλο βιολογικό υλικό που είναι γνωστό ότι προσεγγίζει την ανθεκτικότητα του κερατινοποιημένου ιστού είναι η χιτίνη.[3][4][5] Η κερατίνη απαντά σε δύο τύπους, τις πρωτόγονες, μαλακές μορφές που υπάρχουν σε όλα τα σπονδυλωτά και τις σκληρότερες μορφές που απαντά μόνο στα σαυρόψιδα (ερπετά και πουλιά).
Εμφάνιση στη φύση
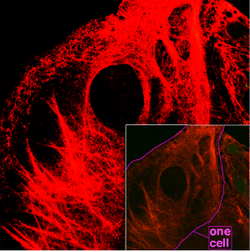
ΕπεξεργασίαΤα νημάτια κερατίνης είναι άφθονα στα κερατινοκύτταρα στο κερατινοποιημένο στρώμα της επιδερμίδας. Επιπλέον, νημάτια κερατίνης υπάρχουν γενικότερα στα επιθηλιακά κύτταρα. Για παράδειγμα, τα επιθηλιακά κύτταρα του θύμου του ποντικού (TECs) είναι γνωστό ότι αντιδρούν με αντισώματα για κερατίνη 5, κερατίνη 8 και κερατίνη 14. Αυτά τα αντισώματα χρησιμοποιούνται ως δείκτες φθορισμού για να διακρίνουν υποσύνολα των TEC σε γενετικές μελέτες του θύμου.
Υπάρχουν δύο ειδών κερατίνες:
- οι α-κερατίνες βρίσκονται σε όλα τα σπονδυλωτά. Βρίσκονται στις τρίχες (συμπεριλαμβανομένου και του μαλλιού), το εξωτερικό στρώμα της επιδερμίδας, τα κέρατα, τα νύχια, και τις οπλές των θηλαστικών,[2] όπως και στις μπαλένες των φαλαινών.
- οι σκληρότερες β-κερατίνες βρίσκονται μόνο στα σαυρόψιδα, δηλαδή όλα τα ζώντα ερπετά και πουλιά. Βρίσκονται στα νύχια και τις φολίδες των ερπετών, στα καύκαλα μερικών ερπετών (όπως οι χελώνες) και στα φτερά, τα ράμφη και τα νύχια των πτηνών.[6] Αυτές οι κερατίνες σχηματίζονται πρωτίστως σε βήτα φύλλα, ωστόσο τα β-φύλλα απαντώται και σε α-κερατίνες.[7]
Οι κερατίνες (που αναφέρονται επίσης ως κυτοκερατίνες) είναι πολυμερή των ενδιάμεσων ινίδια τύπου Ι και τύπου II, τα οποία έχουν βρεθεί μόνο στα γονιδιώματα των χορδωτών. Τα νηματώδη και πολλά άλλα μη χορδωτά ζώα φαίνονται να έχουν μόνο ενδιάμεσα ινίδια τύπου VI, και οι ίνες τους περικλείουν τον πυρήνα και αποτελούνται από λαμίνες.
Δομή
ΕπεξεργασίαΟι πρώτες αλληλουχίες των κερατινών προσδιορίστηκαν το 1982 από τους Χανούκογλου και Φουχς.[8][9] Αυτές οι αλληλουχίες αποκάλυψαν ότι υπάρχουν δύο ξεχωριστές αλλά ομόλογες οικογένειες κερατινών που ονομάστηκαν κερατίνη τύπου Ι και κερατίνες τύπου II.[9] Με ανάλυση των πρωτογενών δομών αυτών των κερατινών και άλλων πρωτεΐνών των ενδιαμέσων ινιδίων, πρότειναν ότι οι κερατίνες και οι άλλες πρωτεΐνες περιέχουν μια κεντρική περιοχή 310 καταλοίπων με τέσσερα τμήματα σε α-ελικοειδή διαμόρφωση τα οποία διαχωρίζονται από τρία μικρά συνδετικά τμήματα συνδετήρα που προβλέπεται ότι έχουν σχήμα β-καμπής.[9] Αυτό το μοντέλο έχει επιβεβαιωθεί από τον προσδιορισμό της κρυσταλλικής δομής μιας ελικοειδούς περιοχής κερατινών.[10]
Τα ινώδη κεράτινα μόρια στρέφονται για να σχηματίσουν ένα πολύ σταθερό, αριστερόστροφο υπερελικοειδές μοτίβο για πολυμερισμό, σχηματίζοντας νήματα που αποτελούνται από πολλαπλά αντίγραφα του μονομερούς κερατίνης.[11] Η κύρια δύναμη που διατηρεί τη δομή των σπειροειδών σπειρών είναι οι υδρόφοβες αλληλεπιδράσεις μεταξύ των απολικών υπολειμμάτων κατά μήκος των ελικοειδών τμημάτων των κερατινών.[12]
Ο περιορισμένος εσωτερικός χώρος είναι ο λόγος για τον οποίο η τριπλή έλικα του (μη σχετικού) δομικού κολλαγόνου, που βρίσκεται στο δέρμα, τους χόνδρους και τα οστά, έχει επίσης υψηλό ποσοστό γλυκίνης. Η πρωτεΐνη συνδετικού ιστού ελαστίνη έχει επίσης υψηλό ποσοστό τόσο γλυκίνης όσο και αλανίνης. Το ινώδες μετάξι, που θεωρείται β-κερατίνη, μπορεί να έχει αυτά τα δύο ως 75-80% του συνόλου, με 10-15% σερίνη, με το υπόλοιπο να έχει ογκώδεις πλευρικές ομάδες. Οι αλυσίδες είναι αντιπαραλληλικές, με εναλλασσόμενο προσανατολισμό C → N.[13] Η υπεροχή των αμινοξέων με μικρές, μη αντιδρώσες πλευρικές ομάδες είναι χαρακτηριστική για τις δομικές πρωτεΐνες, για τις οποίες η κοντινή απόσταση των δεσμών υδρογόνου είναι πιο σημαντική από τη χημική εξειδίκευση.
Γέφυρες δισουλφιδίου
ΕπεξεργασίαΕκτός από τους ενδο- και διαμοριακούς δεσμούς υδρογόνου, το χαρακτηριστικό γνώρισμα των κερατινών είναι η παρουσία μεγάλων ποσοτήτων του θειούχου αμινοξέος κυστεΐνη, που απαιτείται για τις δισουλφιδικές γέφυρες που προσδίδουν επιπλέον αντοχή και ακαμψία με μόνιμο, θερμικά σταθερό δεσμό[14] - με τον ίδιο περίπου τρόπο που οι μη πρωτεϊνικές γέφυρες θείου σταθεροποιούν το βουλκανισμένο καουτσούκ. Τα ανθρώπινα μαλλιά είναι περίπου 14% κυστεΐνη. Οι πικάντικες μυρωδιές της καύσης των μαλλιών και του δέρματος οφείλονται στις σχηματισμένες πτητικές ενώσεις θείου. Η εκτεταμένη δισουλφιδική σύνδεση συμβάλλει στην αδιαλυτότητα των κερατινών, εκτός από έναν μικρό αριθμό διαλυτών όπως παράγοντες διάσπασης ή αναγωγής.
Οι πιο εύκαμπτες και ελαστικές κερατίνες των μαλλιών έχουν λιγότερες δισουλφιδικές γέφυρες σε σχέση με τα νύχια ή τις οπλές, που είναι σκληρότερες. Οι τρίχες και οι άλλες α-κερατίνες αποτελούνται από α-ελικοειδώς περιτυλιγμένες μονές πρωτεϊνικές αλυσίδες (με συνηθισμένους εσωτερικούς δεσμούς υδρογόνου), οι οποίες κατόπιν στριφογυρίζονται περαιτέρω σε υπερ-ελικοειδή σχοινιά που μπορούν να συσπειρωθούν περαιτέρω. Οι β-κερατίνες των ερπετών και των πτηνών έχουν β-πτυχωτά φύλλα στριμμένα μεταξύ τους και σταθεροποιημένα με δισουλφιδικές γέφυρες.
Σχηματισμός ινιδίων
ΕπεξεργασίαΤα νημάτια κερατίνης είναι τα ενδιάμεσα ινίδια. Όπως όλα τα ενδιάμεσα ινίδια, οι πρωτεΐνες κερατίνης σχηματίζουν νηματοειδή πολυμερή σε μια σειρά από βήματα συναρμολόγησης που ξεκινούν με διμερισμό. Τα διμερή συναρμολογούνται σε τετραμερή και οκταμερή και ενδεχομένως, εάν η τρέχουσα υπόθεση ισχύει, σε νημάτια μήκους ικανού να ανασυνδέονται από άκρο σε άκρο σε μακριές ίνες.
Παραπομπές
Επεξεργασία- ↑ Fraser, R.D.B. (1972). Keratins: Their composition, structure and biosynthesis. Bannerstone House: Charles C Thomas. σελίδες 3–6. ISBN 978-0-398-02283-9.
- ↑ 2,0 2,1 Wang, Bin (2016). «Keratin: Structure, mechanical properties, occurrence in biological organisms, and efforts at bioinspiration». Progress in Materials Science 76: 229–318. doi:. https://escholarship.org/uc/item/5sb7q6jp.
- ↑ «Keratin». Webster's Online Dictionary.
- ↑ Vincent, Julian F.V; Wegst, Ulrike G.K (July 2004). «Design and mechanical properties of insect cuticle». Arthropod Structure & Development 33 (3): 187–199. doi:. PMID 18089034.
- ↑ Tombolato, Luca; Novitskaya, Ekaterina E.; Chen, Po-Yu; Sheppard, Fred A.; McKittrick, Joanna (February 2010). «Microstructure, elastic properties and deformation mechanisms of horn keratin». Acta Biomaterialia 6 (2): 319–330. doi:. PMID 19577667.
- ↑ Hickman, Cleveland Pendleton· Roberts, Larry S.· Larson, Allan L. (2003). Integrated principles of zoology . Dubuque, IA: McGraw-Hill. σελ. 538. ISBN 978-0-07-243940-3.
- ↑ Kreplak, L.; Doucet, J.; Dumas, P.; Briki, F. (July 2004). «New Aspects of the α-Helix to β-Sheet Transition in Stretched Hard α-Keratin Fibers». Biophysical Journal 87 (1): 640–647. doi:. PMID 15240497. PMC 1304386. https://archive.org/details/sim_biophysical-journal_2004-07_87_1/page/640.
- ↑ Hanukoglu, I.; Fuchs, E. (Nov 1982). «The cDNA sequence of a human epidermal keratin: divergence of sequence but conservation of structure among intermediate filament proteins». Cell 31 (1): 243–52. doi:. PMID 6186381. https://zenodo.org/record/890743.
- ↑ 9,0 9,1 9,2 Hanukoglu, I.; Fuchs, E. (Jul 1983). «The cDNA sequence of a Type II cytoskeletal keratin reveals constant and variable structural domains among keratins». Cell 33 (3): 915–24. doi:. PMID 6191871. https://zenodo.org/record/890739.
- ↑ Lee, CH.; Kim, MS.; Chung, BM.; Leahy, DJ.; Coulombe, PA. (Jul 2012). «Structural basis for heteromeric assembly and perinuclear organization of keratin filaments». Nat Struct Mol Biol 19 (7): 707–15. doi:. PMID 22705788.
- ↑ Voet, Donald· Voet, Judith· Pratt, Charlotte. «Proteins: Three-Dimensional Structure» (PDF). Fundamentals of Biochemistry. σελ. 158. Ανακτήθηκε στις 1 Οκτωβρίου 2010.
Fibrous proteins are characterized by a single type of secondary structure: a keratin is a left-handed coil of two a helices
- ↑ «Proteopedia: Coiled-coil structure of keratins». Biochem Mol Biol Educ 42 (1): 93–94. Jan 2014. doi:. PMID 24265184.
- ↑ «Secondary Protein». Elmhurst.edu. Αρχειοθετήθηκε από το πρωτότυπο στις 22 Σεπτεμβρίου 2010. Ανακτήθηκε στις 23 Σεπτεμβρίου 2010.
- ↑ «What is Keratin?». WiseGEEK. Ανακτήθηκε στις 11 Μαΐου 2014.