Υδροξώνιο
| Το λήμμα παραθέτει τις πηγές του αόριστα, χωρίς παραπομπές. |
Γενικά στη Χημεία ως οξώνιο χαρακτηρίζεται οποιαδήποτε χημική ένωση στο μόριο της οποίας περιέχεται τρισθενές άτομο Οξυγόνου.
Συνηθέστερα, το ιόν υδρογόνου που βρίσκεται στο νερό προσλαμβάνοντας ένα μόριο αυτού αποτελεί το καλούμενο ιόν του υδροξωνίου, εξ ου και η ταυτόσημη ονομασία υδροξώνιο, ή υδρόνιο αλλά και ως κατιόν υδρογόνου.


Χημικός τύπος
ΕπεξεργασίαΤο ιόν του υδροξωνίου είναι ένα θετικό πολυατομικό ιόν (κατιόν) με χημικό τύπο H3O+.
Στο υδροξώνιο, τα άτομα υδρογόνου ενώνονται με το άτομο οξυγόνου με ομοιοπολικό δεσμό. Μπορούμε να πούμε ότι το ένα από τα τρία άτομα υδρογόνου ενώνεται με ημιπολικό δεσμό με το οξυγόνο, αφού το κοινό ζεύγος ηλεκτρονίων το προσφέρει το οξυγόνο.
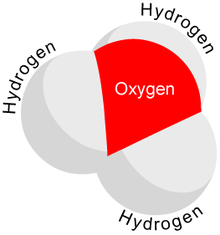
Όπως φαίνεται και στις εικόνες, το υδροξώνιο έχει δομή τριγωνικής πυραμίδας με το άτομο του οξυγόνου στην κορυφή. Η γωνία των δεσμών Η-Ο-Η είναι περίπου 113°. Το Η3Ο+ έχει διπολική ροπή και ανήκει στην ομάδα σημείου C3v.
Σύμφωνα με τη θεωρία των Βrönsted (Δανός χημικός) και Lowry (Άγγλος χημικός) για τα οξέα, το Η3Ο+ είναι ισχυρότατος δότης πρωτονίου δηλαδή πολύ ισχυρό οξύ. Άλλωστε έχει pH = -1,7.
Προέλευση
ΕπεξεργασίαΒασική πηγή υδροξωνίων είναι κυρίως τα οξέα. Ωστόσο, δεδομένου ότι και το νερό μπορεί να συμπεριφερθεί ως οξύ (σύμφωνα με τη θεωρία των Βrönsted και Lowry), υδροξώνια υπάρχουν ακόμα και στο υπερκαθαρό νερό. Αυτή η ειδική περίπτωση κατά την οποία το νερό ιοντίζεται κατά το σχήμα : 2H2Ο ⇄ H3O+ + OH- είναι γνωστή ως αυτο-ιοντισμός του νερού. Πάντως τα υδροξώνια που προκύπτουν έτσι είναι ελάχιστα.
Η ύπαρξη υδροξωνίου στην κατάσταση διάλυσης και μέσα σε μικτά με το νερό οργανικά διαλυτικά μέσα, έχει επιβεβαιωθεί πολλές φορές με τη φασματομετρία IR και NMR, την αγωγιμομετρία και πολαρογραφία. Επίσης, στη στερεή κατάσταση αποδείχθηκε η ύπαρξή του με ακτίνες Χ σε πολλά υδρίδια των οξέων. Έτσι, για παράδειγμα, το κρυσταλλικό πλέγμα του υπερχλωρικού οξέος (HClO4) αποτελείται από τα κατιόντα H3O+ και τα ανιόντα ClO4-. Σαφέστερη όμως απόδειξη ύπαρξης υδροξωνίου είναι με ηλεκτρόλυση διαλύματος υδροβρωμικού οξέος (HBr).
Το υδροξώνιο δεν υπάρχει σε ελεύθερη κατάσταση γιατί είναι εξαιρετικά δραστικό και επιδιαλύεται από το νερό. Πάντως, υδροξώνια εντοπίστηκαν στα διαστρικά νεφελώματα αλλά και στις ουρές των κομητών.
Υδροξώνιο σχηματίζεται όταν εφυδατωθεί ένα κατιόν Η+.
Οξύτητα διαλυμάτων
ΕπεξεργασίαΗ έννοια του pΗ, που αποτελεί μια από τις σημαντικότερες έννοιες της χημείας, στηρίζεται στην ποσότητα υδροξωνίων ενός διαλύματος. Είναι γνωστό ότι : pH = - log[H3O+]. Η συγκέντρωση (Μοριακή κατ' όγκο συγκέντρωση ή Molarity, mol/L) δηλαδή, των υδροξωνίων αποτελεί καθοριστικό παράγοντα για τον χαρακτηρισμό ενός διαλύματος ως όξινου, αλκαλικού ή ουδέτερου.
Πηγές
Επεξεργασία- "Νεώτερον Εγκυκλοπαιδικόν Λεξικόν Ηλίου" τομ.14ος, σελ.928
- Μανουσάκης Γ.Ε. "Γενική και Ανόργανη Χημεία", Τόμοι 1ος και 2ος, Θεσσαλονίκη 1981.
- Γιαννακουδάκης Δ. Α. "Φυσική Χημεία Ιονικών και Ηλεκτροδιακών Δράσεων", Θεσσαλονίκη 1986.
- Morrison R. T., Boyd R. N. "Οργανική Χημεία" Τόμοι 1ος,2ος,3ος, Μετάφραση:Σακαρέλλος-Πηλίδης-Γεροθανάσης, Ιωάννινα 1991.
- Murell J. N., Kettle S. F. A., Tedder J. N. "Ο Χημικός Δεσμός", Μετάφραση Σ. Φαράντος, Ηράκλειο 1992.
- Βασιλικιώτης Γ. Σ. "Ποιοτική Ανάλυση", Θεσσαλονίκη 1980.
- Μπαζάκης Ι. Α. "Γενική Χημεία", Αθήνα.