Τριχλωριούχο αρσενικό
Το τριχλωριούχο αρσενικό είναι μία εξαιρετικά δηλητηριώδης ανόργανη χημική ένωση (LD50 48 mg/kg) με μοριακό τύπο AsCl3 η οποία χρησιμεύει σε πολλές βιομηχανικές εφαρμογές.
| Τριχλωριούχο αρσενικό | |||
|---|---|---|---|

| |||
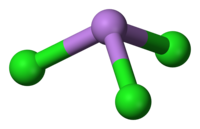
| |||
| Γενικά | |||
| Όνομα IUPAC | Τριχλωροαρσίνη | ||
| Άλλες ονομασίες | Χλωριούχο αρσενικό (ΙΙΙ), βούτυρο του αρσενικού | ||
| Χημικά αναγνωριστικά | |||
| Μοριακή μάζα | 181.2806 g/mol | ||
| Αριθμός CAS | 7784-34-1 | ||
| SMILES | Cl[As](Cl)Cl | ||
| InChI | 1S/AsCl3/c2-1(3)4 | ||
| Αριθμός EINECS | 232-059-5 | ||
| Αριθμός UN | 1560 | ||
| PubChem CID | 24570 | ||
| ChemSpider ID | 22974 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -16.2 °C (257 K) | ||
| Σημείο βρασμού | 130.2 °C (403 K) (υπό πίεση 760 mmHg) | ||
| Πυκνότητα | 2.163 g/cm3 (υγρό) | ||
| Διαλυτότητα στο νερό |
αποσυντίθεται | ||
| Διαλυτότητα σε άλλους διαλύτες |
Διαλυτό σε βενζόλιο, χλωροφόρμιο, τετραχλωράνθρακα, αιθέρα, πτητικά και λιπαρά έλαια, αιθυλική αλκοόλη, υδροχλώριο, υδροβρώμιο | ||
| Ιξώδες | 9.77 x 10-5 Pa s | ||
| Δείκτης διάθλασης , nD |
1.6006 | ||
| Τάση ατμών | 12 mmHg στους 25 °C | ||
| Εμφάνιση | Άχρωμο ελαιώδες υγρό | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
μη αναφλέξιμο | ||
| Επικινδυνότητα | |||
 
| |||
| Πολύ τοξικό (Τ+) Επικίνδυνο για το περιβάλλον (Ν) | |||
| Φράσεις κινδύνου | R23/25, R50/53 | ||
| Φράσεις ασφαλείας | (S1/2), S20/21, S28, S45, S60, S61 | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Ιστορία Επεξεργασία
Το τριχλωριούχο αρσενικό ανακαλύφθηκε το 1648 από τον χημικό Γιόχαν Ρούντολφ Γκλάουμπερ με επίδραση αλατιού (χλωριούχου νατρίου, NaCl) και θειικού οξέος (H2SO4) σε τριοξείδιο του αρσενικού (As2O3) και θέρμανση του μείγματος, οπότε αποστάζεται το τριχλωριούχο αρσενικό: [1]
Η ουσία έγινε γνωστή στους αλχημιστές ως "βούτυρο του αρσενικού".
Παρασκευή Επεξεργασία
Το τριχλωριούχο αρσενικό παρασκευάζεται με επίδραση πυκνού υδροχλωρίου (HCl) σε τριοξείδιο του αρσενικού: [2]
Εναλλακτικά, η ουσία μπορεί να παρασκευαστεί με επίδραση ρεύματος αερίου χλωρίου σε μεταλλικό αρσενικό, μέθοδος όμως δαπανηρότερη της προηγούμενης: [1]
Το προϊόν που αποστάζεται με αυτό τον τρόπο περιέχει διαλυμένο χλώριο και για την απομάκρυνσή του προστίθεται μεταλλικό αρσενικό. [1]
Ιδιότητες Επεξεργασία
Το τριχλωριούχο αρσενικό αποσυντίθεται παρουσία νερού, προς αρσενικώδες οξύ (H3AsO3) και υδροχλώριο, αντίδραση η οποία είναι αμφίδρομη: [1]
Αν υπάρχει περίσσεια πυκνού υδροχλωρίου, τότε το τριχλωριούχο αρσενικό μπορεί να αποσταχθεί αμετάβλητο, ιδιότητα η οποία χρησιμοποιήθηκε για τον ποσοτικό προσδιορισμό του αρσενικού. [1]
Η ουσία αντιδρά με βρωμιούχο κάλιο (KBr) παρέχοντας τριβρωμιούχο αρσενικό:
Και με ιωδιούχο κάλιο (KI) παρέχοντας τριιωδιούχο αρσενικό:
Με χλωριούχα άλατα, το τριχλωριούχο αρσενικό σχηματίζει άλατα τα οποία περιέχουν το αρσενικικό ανιόν [AsO4]-
Η ουσία αποτελεί διαλυτικό μέσο για διάφορες οργανικές ουσίες, όπως το θείο και ο φώσφορος. [1]
Χρήσεις Επεξεργασία
Το τριχλωριούχο αρσενικό χρησιμεύει στη σύνθεση χλωριούχων παραγώγων του αρσενικού τα οποία χρησιμοποιούνται ως ζιζανιοκτόνα, φυτοφάρμακα, παρασιτοκτόνα κ.ο.κ., καθώς και για φαρμακευτικούς σκοπούς.
Βιβλιογραφία Επεξεργασία
- "Μεγάλη Ελληνική Εγκυκλοπαίδεια" Π. Δρανδάκη, τ.Β ', λήμμα "Τριχλωριοῦχον αρσενικόν", σ. 666
