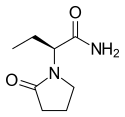
Λεβετιρακετάμη
Η λεβετιρακετάμη, που πωλείται με την επωνυμία Keppra μεταξύ άλλων, είναι φάρμακο που χρησιμοποιείται για τη θεραπεία της επιληψίας.[6] Χρησιμοποιείται για επιληπτικές κρίσεις εστιακές, μυοκλονικές ή τονωτικοκλωνικές και λαμβάνεται είτε από το στόμα ως σύνθεση άμεσης ή παρατεταμένης απελευθέρωσης είτε με ένεση σε φλέβα.[6]
| |||
| Ονομασία IUPAC | |||
|---|---|---|---|
(S)-2-(2-Oxopyrrolidin-1-yl)butanamide | |||
| Κλινικά δεδομένα | |||
| Εμπορικές ονομασίες | Keppra, Elepsia, Spritam, άλλες | ||
| AHFS/Drugs.com | monograph | ||
| MedlinePlus | a699059 | ||
| Δεδομένα άδειας |
| ||
| Κατηγορία ασφαλείας κύησης | |||
| Οδοί χορήγησης | Από το στόμα, ενδοφλεβίως | ||
| Κυκλοφορία | |||
| Κυκλοφορία |
| ||
| Φαρμακοκινητική | |||
| Βιοδιαθεσιμότητα | ~100% | ||
| Πρωτεϊνική σύνδεση | <10% | ||
| Μεταβολισμός | Ενζυμική υδρόλυση της ομάδας ακεταμίδιου | ||
| Βιολογικός χρόνος ημιζωής | 6–8 ώρες | ||
| Απέκκριση | Ούρα | ||
| Κωδικοί | |||
| Αριθμός CAS | 102767-28-2 | ||
| Κωδικός ATC | N03AX14 | ||
| PubChem | CID 5284583 | ||
| IUPHAR/BPS | 6826 | ||
| DrugBank | DB01202 | ||
| ChemSpider | 4447633 | ||
| UNII | 44YRR34555 | ||
| KEGG | D00709 | ||
| ChEBI | CHEBI:6437 | ||
| ChEMBL | CHEMBL1286 | ||
| Χημικά στοιχεία | |||
| Χημικός τύπος | C8H14N2O2 | ||
| Μοριακή μάζα | 170,21 g·mol−1 | ||
O=C1N([C@H](C(=O)N)CC)CCC1 | |||
InChI=1S/C8H14N2O2/c1-2-6(8(9)12)10-5-3-4-7(10)11/h6H,2-5H2,1H3,(H2,9,12)/t6-/m0/s1 Key:HPHUVLMMVZITSG-LURJTMIESA-N | |||
| (verify) | |||
Συχνές ανεπιθύμητες ενέργειες της λεβετιρασετάμης περιλαμβάνουν υπνηλία, ζάλη, αίσθημα κόπωσης και επιθετικότητα.[6] Οι σοβαρές παρενέργειες μπορεί να περιλαμβάνουν ψύχωση, αυτοκτονία και αλλεργικές αντιδράσεις όπως το σύνδρομο Stevens-Johnson ή η αναφυλαξία.[6] Δεν είναι σαφές εάν η λεβετιρακετάμη είναι ασφαλής για χρήση κατά τη διάρκεια της εγκυμοσύνης, αλλά φαίνεται ασφαλής για χρήση κατά το θηλασμό.[1] Η λεβετιρακετάμη είναι το S- εναντιομερές της ετιρακετάμης.[7] Ο μηχανισμός δράσης του δεν είναι ακόμη σαφής.[6]
Η λεβετιρακετάμη εγκρίθηκε για ιατρική χρήση στις Ηνωμένες Πολιτείες το 1999[6] και διατίθεται ως γενόσημο φάρμακο.[8] Το 2017, ήταν το 110ο πιο συχνά συνταγογραφούμενο φάρμακο στις Ηνωμένες Πολιτείες, με περισσότερες από έξι εκατομμύρια συνταγές.[9][10]
Ιατρικές χρήσεις
ΕπεξεργασίαΕστιακή επιληψία
ΕπεξεργασίαΗ λεβετιρασετάμη είναι αποτελεσματική ως φαρμακευτική μονοθεραπεία για νεοδιαγνωσμένη εστιακή επιληψία σε ενήλικες.[11] Μειώνει τις εστιακές κρίσεις κατά 50% ή περισσότερο ως πρόσθετο φάρμακο.[12]
Μερική-σύνθετη επιληψία
ΕπεξεργασίαΗ λεβετιρακετάμη είναι αποτελεσματική ως πρόσθετη θεραπεία για μερική (εστιακή) επιληψία.[13]
Γενικευμένη επιληψία
ΕπεξεργασίαΗ λεβετιρακετάμη είναι αποτελεσματική για τη θεραπεία της γενικευμένης τονικοκλονικής επιληψίας.[14] Έχει εγκριθεί στις Ηνωμένες Πολιτείες ως πρόσθετη θεραπεία για μυοκλονικές και τονωτικοκλονικές κρίσεις.[3] Η λεβετιρασετάμη έχει εγκριθεί στην Ευρωπαϊκή Ένωση ως μονοθεραπεία για την επιληψία σε περίπτωση μερικών επιληπτικών κρίσεων ή ως συμπληρωματική θεραπεία για μερικές, μυοκλονικές και τονωτικοκλωνικές κρίσεις.[15]
Η λεβετιρακετάμη χρησιμοποιείται μερικές φορές εκτός ετικέτας για τη θεραπεία της επιληπτικής κατάστασης (status epilepticus).[16][17]
Πρόληψη επιληπτικών κρίσεων
ΕπεξεργασίαΜε βάση στοιχεία χαμηλής ποιότητας, η λεβετιρασετάμη είναι εξίσου αποτελεσματική με τη φαινυτοΐνη για την πρόληψη πρόωρων επιληπτικών κρίσεων μετά από τραυματικό εγκεφαλικό τραυματισμό.[18] Μπορεί να είναι αποτελεσματικό για την πρόληψη των επιληπτικών κρίσεων που σχετίζονται με υποαραχνοειδείς αιμορραγίες.[19]
Άλλες
ΕπεξεργασίαΗ λεβετιρακετάμη δεν έχει αποδειχθεί χρήσιμη για τη θεραπεία του νευροπαθητικού πόνου[20] ούτε για τη θεραπεία των βασικών τρόμων.[21] Η λεβετιρακετάμη δεν έχει βρεθεί ότι είναι χρήσιμη για τη θεραπεία του αυτισμού,[22][23] αλλά είναι μια αποτελεσματική θεραπεία για μερικές, μυοκλονικές ή τονωτικές-κλωνικές κρίσεις που σχετίζονται με διαταραχή του φάσματος του αυτισμού.[24]
Ειδικές ομάδες
ΕπεξεργασίαΗ λεβετιρασετάμη χαρακτηρίζεται ως φάρμακο κατηγορίας εγκυμοσύνης Γ στις ΗΠΑ.[1] Μελέτες σε θηλυκούς έγκυους αρουραίους έδειξαν μικρές εμβρυϊκές σκελετικές ανωμαλίες όταν δόθηκαν οι μέγιστες συνιστώμενες ανθρώπινες δόσεις λεβετιρακετάμης από το στόμα κατά τη διάρκεια της εγκυμοσύνης και της γαλουχίας.
Η λεβετιρασετάμη μπορεί να χρησιμοποιηθεί με ασφάλεια με προσοχή σε παιδιά άνω των τεσσάρων ετών. Ωστόσο, δεν έχει προσδιοριστεί εάν μπορεί να χορηγηθεί με ασφάλεια σε παιδιά κάτω των 4 ετών.[25]
Παρενέργειες
ΕπεξεργασίαΟι πιο συχνές παρενέργειες της θεραπείας με λεβετιρακετάμη περιλαμβάνουν επιδράσεις στο ΚΝΣ όπως υπνηλία, μειωμένη ενέργεια, πονοκέφαλο, ζάλη, αλλαγές στη διάθεση και δυσκολίες συντονισμού. Αυτές οι ανεπιθύμητες ενέργειες είναι πιο έντονες τον πρώτο μήνα της θεραπείας. Περίπου το 4% των ασθενών εγκατέλειψε τις κλινικές δοκιμές προέγκρισης λόγω αυτών των παρενεργειών.[3]
Περίπου το 13% των ατόμων που λαμβάνουν λεβετιρακετάμη εμφανίζουν ανεπιθύμητα νευροψυχιατρικά συμπτώματα, τα οποία είναι συνήθως ήπια. Αυτά περιλαμβάνουν διέγερση, εχθρότητα, απάθεια, άγχος, συναισθηματική αστάθεια και κατάθλιψη. Σοβαρές ψυχιατρικές ανεπιθύμητες ενέργειες που αντιστρέφονται με τη διακοπή του φαρμάκου εμφανίζονται σε περίπου 1%. Αυτές περιλαμβάνουν ψευδαισθήσεις, σκέψεις αυτοκτονίας ή ψύχωση. Αυτά συνέβησαν κυρίως τον πρώτο μήνα της θεραπείας, αλλά θα μπορούσαν να αναπτυχθούν ανά πάσα στιγμή κατά τη διάρκεια της θεραπείας.[26]
Αν και σπάνια, το σύνδρομο Stevens-Johnson (SJS) και η τοξική επιδερμική νεκρόλυση (TEN), η οποία εμφανίζεται ως επώδυνο επεκτεινόμενο εξάνθημα με ερυθρότητα και φλύκταινες ή/και απολέπιση του δέρματος, έχουν αναφερθεί σε ασθενείς που έλαβαν λεβετιρακετάμη.[27] Η συχνότητα εμφάνισης SJS μετά από έκθεση σε αντιεπιληπτικά όπως η λεβετιρασετάμη είναι περίπου 1 στα 3.000.[28]
Η λεβετιρασετάμη δεν πρέπει να χρησιμοποιείται σε άτομα που είχαν προηγουμένως δείξει υπερευαισθησία στη λεβετιρακετάμη ή σε οποιοδήποτε από τα ανενεργά συστατικά του δισκίου ή του πόσιμου διαλύματος. Τέτοιες αντιδράσεις υπερευαισθησίας περιλαμβάνουν, αλλά δεν περιορίζονται σε ανεξήγητο εξάνθημα με ερυθρότητα ή φουσκάλες επιδερμίδες, δυσκολία στην αναπνοή και σφίξιμο στο στήθος ή τους αεραγωγούς.[3]
Σε μια μελέτη, η συχνότητα μειωμένης οστικής πυκνότητας των ασθενών σε λεβετιρακετάμη ήταν σημαντικά υψηλότερη από εκείνη για άλλα επιληπτικά φάρμακα.[29]
Αυτοκτονία
ΕπεξεργασίαΗ λεβετιρασετάμη, μαζί με άλλα αντιεπιληπτικά φάρμακα, μπορεί να αυξήσει τον κίνδυνο αυτοκτονικής συμπεριφοράς ή σκέψης. Τα άτομα που λαμβάνουν λεβετιρασετάμη πρέπει να παρακολουθούνται στενά για σημάδια επιδείνωσης της κατάθλιψης, αυτοκτονικών σκέψεων ή τάσεων ή για τυχόν μεταβαλλόμενες καταστάσεις συναισθηματικής ή συμπεριφοράς.[3]
Νεφρά και ήπαρ
ΕπεξεργασίαΗ νεφρική δυσλειτουργία μειώνει το ρυθμό αποβολής της λεβετιρακετάμης από το σώμα. Άτομα με μειωμένη νεφρική λειτουργία μπορεί να απαιτούν προσαρμογή της δόσης. Η λειτουργία των νεφρών μπορεί να εκτιμηθεί από τον ρυθμό κάθαρσης κρεατινίνης.[3]
Η προσαρμογή της δόσης της λεβετιρασετάμης δεν είναι απαραίτητη στην ηπατική δυσλειτουργία.[3]
Αλληλεπιδράσεις με άλλα φάρμακα
ΕπεξεργασίαΔεν παρατηρήθηκαν σημαντικές φαρμακοκινητικές αλληλεπιδράσεις μεταξύ της λεβετιρακετάμης ή του κύριου μεταβολίτη της και των συγχορηγούμενων φαρμάκων.[30] Το φαρμακοκινητικό προφίλ της λεβετιρακετάμης δεν επηρεάζεται από φαινυτοΐνη, φαινοβαρβιτάλη, πριμιδόνη, καρβαμαζεπίνη, βαλπροϊκό οξύ, λαμοτριγίνη, γκαμπαπεντίνη, διγοξίνη, αιθινυλοιστραδιόλη ή βαρφαρίνη.[31]
Μηχανισμός δράσης
ΕπεξεργασίαΟ ακριβής μηχανισμός με τον οποίο δρα η λεβετιρακετάμη για τη θεραπεία της επιληψίας είναι άγνωστος. Η λεβετιρακετάμη δεν εμφανίζει φαρμακολογικές δράσεις παρόμοιες με εκείνες των κλασικών αντισπασμωδικών. Δεν αναστέλλει τα κανάλια Na+ που εξαρτώνται από την τάση, δεν επηρεάζει την GABAεργική μετάδοση και δεν συνδέεται με τους GABAεργικούς ή γλουταμιτερικούς υποδοχείς.[32] Ωστόσο, το φάρμακο συνδέεται με το SV2A,[33] μια γλυκοπρωτεΐνη των συναπτικών κυστιδίων, και αναστέλλει τα προσυναπτικά κανάλια ασβεστίου,[34] μειώνοντας την απελευθέρωση νευροδιαβιβαστών και ενεργώντας ως νευροδιαμορφωτής. Αυτό πιστεύεται ότι εμποδίζει την αγωγιμότητα ώθησης στις συνάψεις.[35]
Φαρμακοκινητική
ΕπεξεργασίαΗ απορρόφηση των δισκίων λεβετιρακετάμης και του πόσιμου διαλύματος είναι ταχεία και ουσιαστικά πλήρης. Η βιοδιαθεσιμότητα της λεβετιρακετάμης πλησιάζει το 100 τοις εκατό και η επίδραση της τροφής στην απορρόφηση είναι μικρή.[3]
Ο όγκος κατανομής της λεβετιρακετάμης είναι παρόμοιος με το συνολικό νερό του σώματος. Η λεβετιρακετάμη δεσμεύεται μέτρια στις πρωτεΐνες του πλάσματος (λιγότερο από 10%).[3]
Η λεβετιρακετάμη δεν υφίσταται εκτεταμένο μεταβολισμό και οι μεταβολίτες που σχηματίζονται δεν είναι δραστικοί και δεν ασκούν φαρμακολογική δράση. Ο μεταβολισμός της λεβετιρακετάμης δεν γίνεται από τα ένζυμα του κυτοχρώματος P450 του ήπατος, αλλά μέσω άλλων μεταβολικών οδών όπως η υδρόλυση και η υδροξυλίωση.[3]
Σε άτομα με φυσιολογική νεφρική λειτουργία, η λεβετιρακετάμη αποβάλλεται από το σώμα κυρίως από τα νεφρά με περίπου το 66% του αρχικού φαρμάκου να μεταφέρεται αμετάβλητο στα ούρα. Ο χρόνος ημιζωής της λεβετιρασετάμης στο πλάσμα σε ενήλικες είναι περίπου 6 έως 8 ώρες.[3]
Παραπομπές
Επεξεργασία- ↑ 1,0 1,1 1,2 1,3 «Levetiracetam Use During Pregnancy». Drugs.com. Ανακτήθηκε στις 5 Μαρτίου 2019.
- ↑ «Keppra 100 mg/ml concentrate for solution for infusion - Summary of Product Characteristics (SmPC)». (emc). Ανακτήθηκε στις 9 Σεπτεμβρίου 2020.
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 «Keppra- levetiracetam tablet, film coated Keppra- levetiracetam solution». DailyMed. 5 Νοεμβρίου 2019. Ανακτήθηκε στις 9 Σεπτεμβρίου 2020.
- ↑ «Keppra XR- levetiracetam tablet, film coated, extended release». DailyMed. 4 Νοεμβρίου 2019. Ανακτήθηκε στις 9 Σεπτεμβρίου 2020.
- ↑ «Keppra- levetiracetam injection, solution, concentrate». DailyMed. 4 Νοεμβρίου 2019. Ανακτήθηκε στις 9 Σεπτεμβρίου 2020.
- ↑ 6,0 6,1 6,2 6,3 6,4 6,5 «Levetiracetam Monograph for Professionals». Drugs.com (στα Αγγλικά). AHFS. Ανακτήθηκε στις 14 Ιανουαρίου 2019.
- ↑ Cavanna, Andrea E. (2018). Behavioural Neurology of Anti-Epileptic Drugs: A Practical Guide. Oxford University Press. σελ. 17. ISBN 9780198791577.
- ↑ British national formulary: BNF 76 (76 έκδοση). Pharmaceutical Press. 2018. σελ. 319. ISBN 9780857113382.
- ↑ «The Top 300 of 2020». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Levetiracetam - Drug Usage Statistics». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Antiepileptic monotherapy in newly diagnosed focal epilepsy. A network meta-analysis». Acta Neurol. Scand. 139 (1): 33–41. January 2019. doi:. PMID 30194755.
- ↑ Mbizvo, Gashirai K; Dixon, Pete; Hutton, Jane L; Marson, Anthony G (2012). «Levetiracetam add-on for drug-resistant focal epilepsy: An updated Cochrane Review». Cochrane Database of Systematic Reviews (9): CD001901. doi:. PMID 22972056.
- ↑ «Efficacy of antiepileptic drugs in the adjunctive treatment of refractory partial-onset seizures: Meta-analysis of pivotal trials». Epilepsy Res. 143: 120–129. July 2018. doi:. PMID 29784458.
- ↑ «Antiepileptic drug monotherapy for epilepsy: a network meta-analysis of individual participant data». Cochrane Database Syst Rev 12: CD011412. December 2017. doi:. PMID 29243813.
- ↑ BNF 59. BMA & RPSGB. 2010.
- ↑ Brophy, Gretchen M.; Bell, Rodney; Claassen, Jan; Alldredge, Brian; Bleck, Thomas P.; Glauser, Tracy; Laroche, Suzette M.; Riviello, James J. και άλλοι. (2012). «Guidelines for the Evaluation and Management of Status Epilepticus». Neurocritical Care 17 (1): 3–23. doi:. PMID 22528274.
- ↑ Meierkord, H.; Boon, P.; Engelsen, B.; Göcke, K.; Shorvon, S.; Tinuper, P.; Holtkamp, M. (2010). «EFNS guideline on the management of status epilepticus in adults». European Journal of Neurology 17 (3): 348–55. doi:. PMID 20050893.
- ↑ «Should Levetiracetam or Phenytoin Be Used for Posttraumatic Seizure Prophylaxis? A Systematic Review of the Literature and Meta-analysis». Neurosurgery 79 (6): 775–782. December 2016. doi:. PMID 27749510.
- ↑ Shah, Dharmen; Husain, Aatif M. (2009). «Utility of levetiracetam in patients with subarachnoid hemorrhage». Seizure 18 (10): 676–9. doi:. PMID 19864168.
- ↑ Crawford-Faucher, A; Huijon, R. M. (2015). «The Role of Levetiracetam in Treating Chronic Neuropathic Pain Symptoms». American Family Physician 92 (1): 23–4. PMID 26132123. http://www.aafp.org/link_out?pmid=26132123.
- ↑ Zesiewicz, T. A.; Elble, R. J.; Louis, E. D.; Gronseth, G. S.; Ondo, W. G.; Dewey, R. B.; Okun, M. S.; Sullivan, K. L. και άλλοι. (2011). «Evidence-based guideline update: Treatment of essential tremor: Report of the Quality Standards Subcommittee of the American Academy of Neurology». Neurology 77 (19): 1752–5. doi:. PMID 22013182.
- ↑ Volkmar, Fred; Siegel, Matthew; Woodbury-Smith, Marc; King, Bryan; McCracken, James; State, Matthew (2014). «Practice Parameter for the Assessment and Treatment of Children and Adolescents with Autism Spectrum Disorder». Journal of the American Academy of Child & Adolescent Psychiatry 53 (2): 237–57. doi:. PMID 24472258.
- ↑ Hirota, Tomoya; Veenstra-Vanderweele, Jeremy; Hollander, Eric; Kishi, Taro (2013). «Antiepileptic Medications in Autism Spectrum Disorder: A Systematic Review and Meta-Analysis». Journal of Autism and Developmental Disorders 44 (4): 948–57. doi:. PMID 24077782.
- ↑ Frye, Richard; Rossignol, Daniel; Casanova, Manuel F.; Brown, Gregory L.; Martin, Victoria; Edelson, Stephen; Coben, Robert; Lewine, Jeffrey και άλλοι. (2013). «A review of traditional and novel treatments for seizures in autism spectrum disorder: Findings from a systematic review and expert panel». Frontiers in Public Health 1: 31. doi:. PMID 24350200.
- ↑ «Advancements in the treatment of epilepsy». Annu. Rev. Med. 59: 503–23. February 2008. doi:. PMID 17883367. https://seizure.mgh.harvard.edu/wp-content/uploads/Advances-in-the-Treatment-of-Epilepsy.pdf.
- ↑ Gambardella, Antonio (2008). «Monotherapy for partial epilepsy: Focus on levetiracetam». Neuropsychiatric Disease and Treatment 4 (1): 33–8. doi:. PMID 18728811.
- ↑ Zou, Li-Ping; Ding, Chang-Hong; Song, Zhen-Jiang; Li, Xiao-Feng (2012). «Stevens–Johnson syndrome induced by levetiracetam». Seizure 21 (10): 823–5. doi:. PMID 23036769.
- ↑ Griebel, May L. (1998). «Acute Management of Hypersensitivity Reactions and Seizures». Epilepsia 39: S17–21. doi:. PMID 9798757.
- ↑ Beniczky, Simona Alexandra; Viken, Janina; Jensen, Lars Thorbjørn; Andersen, Noémi Becser (2012). «Bone mineral density in adult patients treated with various antiepileptic drugs». Seizure 21 (6): 471–2. doi:. PMID 22541979.
- ↑ Browne, T. R.; Szabo, G. K.; Leppik, I. E.; Josephs, E.; Paz, J.; Baltes, E.; Jensen, C. M. (2000). «Absence of Pharmacokinetic Drug Interaction of Levetiracetam with Phenytoin in Patients with Epilepsy Determined by New Technique». The Journal of Clinical Pharmacology 40 (6): 590–5. doi:. PMID 10868309. https://archive.org/details/sim_journal-of-clinical-pharmacology_2000-06_40_6/page/590.
- ↑ Gidal, Barry E.; Baltès, Eugène; Otoul, Christian; Perucca, Emilio (2005). «Effect of levetiracetam on the pharmacokinetics of adjunctive antiepileptic drugs: A pooled analysis of data from randomized clinical trials». Epilepsy Research 64 (1–2): 1–11. doi:. PMID 15823510.
- ↑ «Mechanisms of levetiracetam in the control of status epilepticus and epilepsy». Front Neurol 5: 11. 2014. doi:. PMID 24550884.
- ↑ «The synaptic vesicle protein SV2A is the binding site for the antiepileptic drug levetiracetam». Proc Natl Acad Sci USA 101 (26): 9861–6. June 2004. doi:. PMID 15210974. Bibcode: 2004PNAS..101.9861L.
- ↑ «The Synaptic Vesicle Glycoprotein 2A Ligand Levetiracetam Inhibits Presynaptic Ca2+ Channels through an Intracellular Pathway». Mol. Pharmacol. 82 (2): 199–208. August 2012. doi:. PMID 22554805.
- ↑ Rogawski, MA (June 2006). «Diverse mechanisms of antiepileptic drugs in the development pipeline». Epilepsy Research 69 (3): 273–94. doi:. PMID 16621450.